题目内容
某研究性学习小组将一定浓度的Na2CO3溶液滴入MgSO4溶液中得到白色沉淀。甲同学认为两者反应只生成MgCO3一种沉淀;乙同学认为这两者相互促进水解,只生成Mg(OH)2一种沉淀;丙同学认为生成MgCO3和Mg(OH)2两种沉淀。(查阅资料知:MgCO3和Mg(OH)2均不带结晶水)
(1)按照乙同学的理解Na2CO3溶液和MgSO4溶液反应的化学反应方程式为___________________;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
(2)请用下图所示装置,选择合适的实验装置和必要的试剂,证明沉淀物中只有碳酸镁。
①各装置连接顺序为__________________(用装置编号表示);
②装置C中装有试剂的名称是______________;
③能证明生成物中只有MgCO3的实验现象是_______。
(3)若Mg(OH)2和MgCO3两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。
实验结束时通入过量的空气的作用是______________________________。
A装置和E装置的共同作用是__________________________。
③实验过程中测定的数据有:W1:样品的质量,W2:反应后装置B中残渣的质量,W3:反应生成水的质量,W4:反应生成二氧化碳的质量,为了测定其组成,至少需要其中____个数据,请将可能的组合填入下表中(每个空格中填一种组合)。
(1)Na2CO3+MgSO4+H2O=Mg(OH)2↓+Na2SO4+CO2↑.(2) ①A→C→B. ②无水硫酸铜③装置B中澄清的石灰水变浑浊,装置C中无水硫酸铜不变蓝色。(3)①将装置B中滞留的水蒸气和CO2吹入后面的装置中以完全吸收。②吸收空气中的水蒸气和和CO2防止对实验造成干扰。③2可能组合为:W1W2W1W3W1W4W2W3W2W4W3W4。
解析试题分析:(1)根据题意可得方程式为Na2CO3+MgSO4+H2O=Mg(OH)2↓+Na2SO4+CO2↑.(2)用A加热物质,然后用B通过检验水的存在来确定是否含有氢元素,最后用C澄清的石灰水来确定二氧化碳的存在及含量。(3)采用该装置,实验结束时通入过量的空气是为了将装置B中滞留的水蒸气和CO2吹入后面的装置中以完全吸收。A、E的作用是吸收空气中的水蒸气和和CO2防止对实验造成干扰根据给定的物质质量等数据可看出要想确定物质组成至少需要两个数据,这些可能的组合为W1W2W1W3W1W4W2W3W2W4W3W4。
考点:考查实验法来确定物质组成应该注意的事项等相关知识。

 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| | 苯 | 溴 | 溴苯 |
| 密度/g·cm-3 | 0. 88 | 3. 10 | 1. 50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
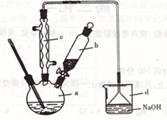
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液溴。向a中滴人几滴液溴,有白雾产生,是因为生成了 气体。继续滴加至液溴滴完。装置d的作用是_________________________ 。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入l0mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mLl0%的NaOH溶液、l0mL水洗涤。NaOH溶液洗涤的作用是
。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是
。
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯下列操作中必须的是 (填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填人正确选项前的字母)。
A.25mL B.50mL C.250mL D.500mL












