题目内容
(8分)在25℃时,向100ml含氯化氢14.6g的盐酸溶液里放人5.60g纯铁粉(不考虑反应前后溶液体积变化),反应开始至2min末,收集到1.12L(标准状况)氢气。在此之后,又经过4min,铁粉完全溶解。则:
(1)在前2min内用FeCl2表示的平均化学反应速率是_______
(2)在后4min内用HCl表示的平均化学反应速率是_______
(3)前2min与后4min相比,反应速率较快的是 ________,其原因是_____
(1)在前2min内用FeCl2表示的平均化学反应速率是_______
(2)在后4min内用HCl表示的平均化学反应速率是_______
(3)前2min与后4min相比,反应速率较快的是 ________,其原因是_____
0.25 mol/L·min 0.25 mol/L·min 前两分钟,前两分钟盐酸浓度较大
涉及反应:Fe+2HCl=FeCl2+H2↑
铁粉的物质的量为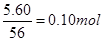 ,2min末,得到氢气
,2min末,得到氢气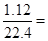 0.05mol
0.05mol
(1)前2min内生成FeCl2的物质的量为0.05mol,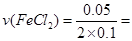 0.25 mol/L
0.25 mol/L
(2)后4min内,溶解的铁为0.1mol—0.05mol=0.05mol,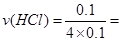 0.25 mol/L
0.25 mol/L
(3)根据方程式系数比可知后4min内,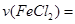 0.125 mol/L,即前2min内反应速率快,主要是由于前两分钟盐酸浓度较大
0.125 mol/L,即前2min内反应速率快,主要是由于前两分钟盐酸浓度较大
铁粉的物质的量为
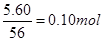 ,2min末,得到氢气
,2min末,得到氢气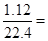 0.05mol
0.05mol(1)前2min内生成FeCl2的物质的量为0.05mol,
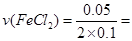 0.25 mol/L
0.25 mol/L(2)后4min内,溶解的铁为0.1mol—0.05mol=0.05mol,
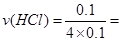 0.25 mol/L
0.25 mol/L(3)根据方程式系数比可知后4min内,
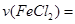 0.125 mol/L,即前2min内反应速率快,主要是由于前两分钟盐酸浓度较大
0.125 mol/L,即前2min内反应速率快,主要是由于前两分钟盐酸浓度较大
练习册系列答案
相关题目
 CH3OH(g)+H2O(g) 。
CH3OH(g)+H2O(g) 。
 CH3OH (g) ΔH=-90.8 kJ·mol-1
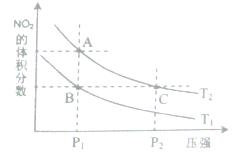
CH3OH (g) ΔH=-90.8 kJ·mol-1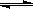 CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如右图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如右图所示。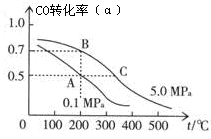
 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
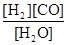 ,它所对应的化学反应为:
,它所对应的化学反应为: 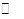 2C0(g),K1 ①
2C0(g),K1 ① K1、K2、K3,之间的关系是: ,反应①的平衡常数K随温度的升高而 (增大/减小/不变)。
K1、K2、K3,之间的关系是: ,反应①的平衡常数K随温度的升高而 (增大/减小/不变)。
 2Z ,达到平衡后, X的转化率不可能为
2Z ,达到平衡后, X的转化率不可能为