题目内容
【题目】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)已知FeCl3在反应中得到电子,则该反应的还原剂是__________。
(2)将上述反应设计成的原电池如图所示,请回答下列问题:
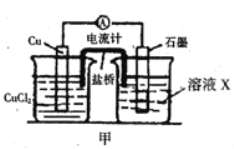
①电解质溶液X是_____;
②Cu电极上发生的电极反应式为_____;
③原电池工作时,盐桥中的___离子(填“K+”或“Cl—”)不断进入X溶液中。
【答案】Cu FeCl3 Cu-2e-=Cu2+ K+
【解析】
(1)氯化铁具有强氧化性,铜能被氯化铁氧化,所以铜做还原剂,故答案为:Cu;
(2)①氯化铁具有强氧化性,铜能被氯化铁氧化,所以反应为2FeCl3+Cu=CuCl2+2FeCl2,则FeCl3溶液为电解质溶液,故答案为:FeCl3;
②Cu作负极,失电子发生氧化反应,电极反应为Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
③石墨作正极,放电时,电解质溶液中阳离子向正极移动,所以盐桥中的K+移向X溶液,故答案为:K+;

【题目】下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验KIO3中的碘元素 | 取少量KIO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液 |
B | 检验石油裂解气中的乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
C | 比较HClO和CH3COOH的酸性强弱 | 室温下,用pH计测定饱和的NaClO溶液和饱和的 |
D | 硅酸胶体的制备 | 向 |
A.AB.BC.CD.D
【题目】已知下列操作和现象,所得结论正确的是
选项 | 操作和现象 | 结论 |
A | 其他条件不变,缩小H2(g)+I2 (g) | 增大压强,平衡逆向移动 |
B | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热;未出现银镜 | 蔗糖未水解 |
C | 向蛋白质溶液中加入CuSO4溶液和Na2SO4饱和溶液,均产生白色沉淀 | 蛋白质均发生了变性 |
D | 其他条件相同时,Na2S2O3溶液和稀H2SO4反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
A. AB. BC. CD. D