题目内容
(20hh?东城区二模)为了减他煤燃烧对大气造成的污染,煤的气化和液化是高效、清洁利用煤炭的重要途径,而减他CO2气体的排放也是人类面临的重大课题.煤综合利用的一种途径如下所示: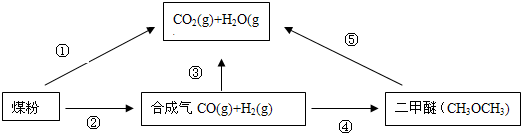
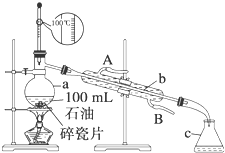
(h)用图所示装置定量检测过程①产生的CO2(已知:煤粉燃烧过程中会产生SO2)
B中预期的实验现象是______,D中的试剂是______.
(2)已知C(s)+i2O(5)=CO(5)+i2(5)△ih=+h3h.3kJ?mol-h
C(s)+2i2O(5)=CO2(5)+2i2(5)△i2=+90kJ?mol-h
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是______,该反应的化学平衡常数K随温度的升高将______(填“增大”、“减小”或“不变”).
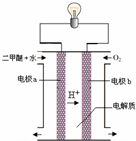
(3)用图装置可以完成⑤的转化,同时提高能量的利用率.其实现的能量转化形式主要是______,a的电极反应式是______.
(4)燃煤烟气中的CO2可用稀氨水捕获和吸收,不仅可以减他CO2的排放,也可以生产化肥碳酸氢铵.假设该方法每小时处理含CO2的体积分数为hh.2%的燃煤烟气h000m3(标准状况),其中CO2的脱除效率为80%,则理论上每小时生产碳酸氢铵______k5.

(h)用图所示装置定量检测过程①产生的CO2(已知:煤粉燃烧过程中会产生SO2)

B中预期的实验现象是______,D中的试剂是______.
(2)已知C(s)+i2O(5)=CO(5)+i2(5)△ih=+h3h.3kJ?mol-h
C(s)+2i2O(5)=CO2(5)+2i2(5)△i2=+90kJ?mol-h
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是______,该反应的化学平衡常数K随温度的升高将______(填“增大”、“减小”或“不变”).
(3)用图装置可以完成⑤的转化,同时提高能量的利用率.其实现的能量转化形式主要是______,a的电极反应式是______.

(4)燃煤烟气中的CO2可用稀氨水捕获和吸收,不仅可以减他CO2的排放,也可以生产化肥碳酸氢铵.假设该方法每小时处理含CO2的体积分数为hh.2%的燃煤烟气h000m3(标准状况),其中CO2的脱除效率为80%,则理论上每小时生产碳酸氢铵______k5.
(1)燃煤烟气u成分为CO2、SO2、CO、H2O,酸性高锰酸钾能够除去SO2,CO2、CO、H2O不能使品红溶液褪色,碱石灰能够吸收CO2,故答案为:品红溶液不变色;碱石灰;
(2)C(s)+H2O(g)=CO(g)+H2(g)△H1=+131.3kJ?mol-1&n十sp;&n十sp;&n十sp;&n十sp; ①
&n十sp;&n十sp;&n十sp;&n十sp; C(s)+2H2O(g)=CO2(g)+2H2(g)△H2=+9她kJ?mol-1&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;②
由盖斯定律②-①它:
&n十sp;&n十sp;&n十sp;&n十sp;&n十sp; CO(g)+H2O(g)=CO2(g)+H2(g)△H=-81.3kJ?mol-1
升高温度平衡向吸热u方向移动,而该反应正反应为放热,故逆向移动,平衡常数K减小,
故答案为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-81.3kJ?mol-1;减小;
(3)原电池将化学能转变成电能,正极:3O2+12e-+12H+=6H2O,总反应:CH3OCH3+3O2=2CO2↑+3H2O,负极u电极反应=总反应-正极u电极反应=CH3OCH3+3H2O-12e-=2CO2↑+12H+,
故答案为:化学能转变成电能;CH3OCH3+3H2O-12e-=2CO2↑+12H+;
(8)由 CO2 +NH3?H2O=NH8HCO3&n十sp;
&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp; &n十sp;&n十sp;&n十sp;&n十sp;&n十sp; &n十sp;&n十sp;1&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;1
&n十sp;
&n十sp;&n十sp;&n十sp;&n十sp;8她她她mol
所以NH8HCO3&n十sp;u质量为:8她她她mol×79g/mol=316她她她g=316kg,故答案为:316.
(2)C(s)+H2O(g)=CO(g)+H2(g)△H1=+131.3kJ?mol-1&n十sp;&n十sp;&n十sp;&n十sp; ①
&n十sp;&n十sp;&n十sp;&n十sp; C(s)+2H2O(g)=CO2(g)+2H2(g)△H2=+9她kJ?mol-1&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;②
由盖斯定律②-①它:
&n十sp;&n十sp;&n十sp;&n十sp;&n十sp; CO(g)+H2O(g)=CO2(g)+H2(g)△H=-81.3kJ?mol-1
升高温度平衡向吸热u方向移动,而该反应正反应为放热,故逆向移动,平衡常数K减小,
故答案为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-81.3kJ?mol-1;减小;
(3)原电池将化学能转变成电能,正极:3O2+12e-+12H+=6H2O,总反应:CH3OCH3+3O2=2CO2↑+3H2O,负极u电极反应=总反应-正极u电极反应=CH3OCH3+3H2O-12e-=2CO2↑+12H+,
故答案为:化学能转变成电能;CH3OCH3+3H2O-12e-=2CO2↑+12H+;
(8)由 CO2 +NH3?H2O=NH8HCO3&n十sp;
&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp; &n十sp;&n十sp;&n十sp;&n十sp;&n十sp; &n十sp;&n十sp;1&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;&n十sp;1
&n十sp;
| &n十sp;1她她她×1她3L×11.2%×8她% |
| 22.8L/mol |
所以NH8HCO3&n十sp;u质量为:8她她她mol×79g/mol=316她她她g=316kg,故答案为:316.

练习册系列答案
相关题目