��Ŀ����
����Ŀ�����й��ڼס��ҡ��������ĸ�ͼ���˵���У�����ȷ����
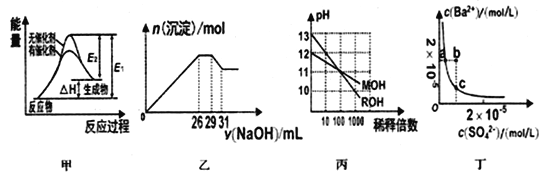
A. ���üױ�ʾij���淴Ӧ�������仯��˵�������ܸı������淴Ӧ�Ļ��
B. ͼ�ұ�ʾ�ں�Mg2+��Al3+��NH4+��Cl-����Һ�У�����һ��Ũ��NaOH��Һʱ���ɳ�����ͼ����ͼ�ɵ�ԭ��Һ�У�n(Mg2+):n(Al3+):n(NH4+)=10:2:3
C. ͼ����ʾMOH��ROH����һԪ�����Һ�ֱ��ˮϡ��ʱ��pH�仯����ͼ�ɵü��ԣ�ROH>MOH
D. ͼ����ʾij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ�����ߣ������Na2SO4����ʹ��Һ��a��䵽b��
���𰸡�D
��������A�����üױ�ʾij���淴Ӧ�������仯�������ı䷴Ӧ���ʣ�������Ϊ�����ܸı������淴Ӧ�Ļ�ܣ���A��ȷ��B����1mLNaOH��Һ��NaOH�����ʵ���Ϊamol�����ͼʾ�п�֪n(NH4+)=3amol��n(Al3+)=2amol����n(Mg2+)=(26amol-2amol��3)��2=10amol����ԭ��Һ�У�n(Mg2+):n(Al3+):n(NH4+)=10:2:3����B��ȷ��C������ϡ�����дٽ����룬�����ǿ��ϡ����ͬ�ı�����pH�仯���Ϊǿ�����ͼ�ɵü��ԣ�ROH>MOH����C��ȷ��D���¶�һ��ʱ����BaSO4ˮ�еij����ܽ�ƽ���У�����Na2SO4��ʹ��Һ��SO42-Ũ������ƽ�������ƶ���Ba2+��С��������a��䵽b�㣬��D����ΪD��

����Ŀ�������ǹ�ũҵ�����в��ɻ�ȱ�����ʣ��о���ȡ�����Ļ�������Ƿ���
��1���ڳ��¡���ѹ�����������£�N2�ڲ�������Fe2O3��TiO2����������ˮ�������з�Ӧ:
N2(g)+3H2O(l)![]() 2NH3(g)+
2NH3(g)+![]() O2(g) ��H=a kJ mol-1 ��
O2(g) ��H=a kJ mol-1 ��
Ϊ��һ���о�����NH3�����ʵ������¶ȵĹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������£�
T/K | 303 | 313 | 323 |
n(NH3)/(l0-2 mol) | 4.8 | 5.9 | 6.0 |
�˷�Ӧ��a_________0����S________0�����>����<���� = ����
��2�������¶Ⱥ�ѹǿ�£���2 L�ĺ����ܱ������кϳɰ���:N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4 kJ mol-1���ڷ�Ӧ�����з�Ӧ�������������ʵ�����ʱ��ı仯��ͼ��ʾ��
2NH3(g) ��H=-92.4 kJ mol-1���ڷ�Ӧ�����з�Ӧ�������������ʵ�����ʱ��ı仯��ͼ��ʾ��

�� 0��10 min�ڣ���NH3��ʾ��ƽ����Ӧ����Ϊ_________��
�� ��10��20 min�ڣ�NH3Ũ�ȱ仯��ԭ�������_______��
A��������� B����С������� C�������¶� D������NH3�����ʵ���
�� �ڷ�Ӧ������25 minʱ�����߷����仯��ԭ����____________���ﵽ�ڶ���ƽ��ʱ����ƽ���ƽ�ⳣ��K2______K1���>����<���� = ����