题目内容
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O。则生成的盐溶液中NaNO3的物质的量为( )
| A.0.2 mol | B.0.4 mol | C.0.6 mol | D.0.8 mol |
A
试题分析:n(Cu)=" 51.2" g÷64g/mol=0.8mol.Cu失去电子的物质的量是0.8×2="1.6mol." 硝酸得到电子产生氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,,n(NaOH)=1mol.由于氮的氧化物都转化为NaNO3或NaNO2.n(N)n(Na)=1:1,所以n(N2O4)=0.2mol;n(NO+NO2)=0.6mol..假设收集到氮的氧化物(含NO、N2O4、NO2)的混合物0.8 mol,含有二氧化氮的物质的量为a ,一氧化氮的物质的量为(0.6-a)mol, n(N2O4)=0.2mol.根据电子守恒可得:1×a+3×(0.6-a)+2×0.2=1.6.解得a=0.3mol.因为N2O4
 2NO2.
2NO2.收集到氮氧化物也就相当于是n(NO2)=0.3+2×0.2=0.7mol.,n(NO)=0.3mol.。结合两个方程式可知发生第二个反应的二氧化氮、一氧化氮的物质的量都是0.3mol,发生第一个反应的二氧化氮物质的量为0.4mol.所以产生NaNO30.2mol, 产生NaNO20.2mol+0.3mol="0.8mol."

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
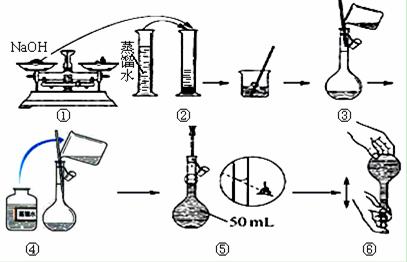

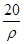 mol·L-1
mol·L-1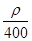 mol·L-1
mol·L-1