题目内容
(11分)阅读下面的信息,推断元素及有关物质,按要求回答物质:
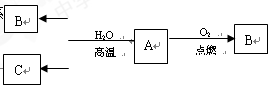
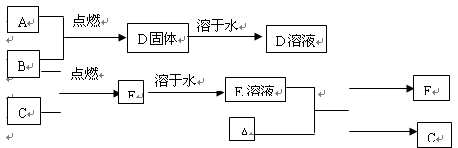
信息①:X、Y、Z、W是常见的短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。
(1)根据信息①,X一定不是 (填序号)
信息②:上述四种元素的单质均能在足量的氧气中燃烧,生成的四种氧化物中,有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液,氧化物的相对分子质量都大于26。
(2)这四种元素中是否有一种是铝元素?为什么?
; 。
信息③:向上述四种元素单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)白色沉淀物的化学式为 。
信息④:向上述四种元素单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸溶液,最终溶液中析出白色沉淀。
(4)生成白色沉淀物的离子方程式为 。
。
信息⑤:上述四种元素中,X与W同主族。
(5)X与浓硫酸反应的化学方程式为 。
信息①:X、Y、Z、W是常见的短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。
(1)根据信息①,X一定不是 (填序号)
| A.氢 | B.碳 | C.氧 | D.硫 |
(2)这四种元素中是否有一种是铝元素?为什么?
; 。
信息③:向上述四种元素单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)白色沉淀物的化学式为 。
信息④:向上述四种元素单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸溶液,最终溶液中析出白色沉淀。
(4)生成白色沉淀物的离子方程式为
 。
。信息⑤:上述四种元素中,X与W同主族。
(5)X与浓硫酸反应的化学方程式为 。
(1)AD(2分)
(2)是(1分),因为有一种氧化物既能溶于酸,又能溶于碱,是两性氧化物(2分)。
(3)Mg(OH)2(2分)
(4)SiO32-+2H+=H2SiO3↓(2分)
(5)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)
(2)是(1分),因为有一种氧化物既能溶于酸,又能溶于碱,是两性氧化物(2分)。
(3)Mg(OH)2(2分)
(4)SiO32-+2H+=H2SiO3↓(2分)
(5)C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)略

练习册系列答案
相关题目
 两容积相等的密闭容器。
两容积相等的密闭容器。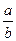 ________
________ 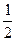 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
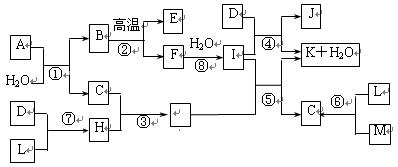
 (1)写出G的电子式 ,
(1)写出G的电子式 ,