题目内容
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 是短周期元素,
是短周期元素,![]() 元素原子的最外层电子未达到8电子稳定结构,工业上通过分离液态空气获得其单质;
元素原子的最外层电子未达到8电子稳定结构,工业上通过分离液态空气获得其单质;![]() 元素原子最外电子层上
元素原子最外电子层上![]() 、
、![]() 电子数相等;
电子数相等;![]() 元素的
元素的![]() 价阳离子的核外电子排布与氖原子相同;
价阳离子的核外电子排布与氖原子相同;![]() 元素原子的
元素原子的![]() 层有1个未成对的
层有1个未成对的![]() 电子。下列有关这些元素性质的说法一定正确的是( )
电子。下列有关这些元素性质的说法一定正确的是( )
A.![]() 元素的简单氢化物的水溶液显碱性
元素的简单氢化物的水溶液显碱性
B.![]() 元素的离子半径大于
元素的离子半径大于![]() 元素的离子半径
元素的离子半径
C.![]() 元素的单质在一定条件下能与
元素的单质在一定条件下能与![]() 元素的单质反应
元素的单质反应
D.![]() 元素的最高价氧化物在常温下不是气态
元素的最高价氧化物在常温下不是气态
【答案】C
【解析】
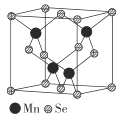
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质,X可能为O,也可能为N元素;Z元素+2价阳离子的核外电子排布与氖原子相同,则Z元素的质子数为10+2=12,故Z为Mg元素;Y元素原子最外电子层上s、p电子数相等,外围电子排布为ns2np2,处于ⅣA族,且属于短周期元素,所以Y为C或Si元素;W元素原子的M层有1个未成对的p电子,外围电子排布为3s23p1或3s23p5,W为Al或Cl,据此分析作答。
A. X可能为O或N,氢化物可以是H2O、NH3,水是中性,故A错误;
B. 若W为Cl,镁离子与氯离子最外层电子数相同,电子层越多离子半径越大,镁离子半径小于氯离子半径,若W为Al,镁离子与铝离子电子层结构相同,核电荷数越大,离子半径越小,镁离子半径大于铝离子半径,故B错误;
C. Mg在氮气中燃烧生成Mg3N2,在氧气中燃烧生成氧化镁,故C正确;
D. Y为C或Si元素,其最高价氧化物分别为二氧化碳或二氧化硅,二氧化硅在常温下为固体,非气体,而二氧化碳晶体属于分子晶体,常温下为气体,故D错误;
故选C。

练习册系列答案
相关题目