题目内容
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
【答案】D
【解析】
A、H2S是二元弱酸,H2S ![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-,c(H+)>c(H2S),故错误;B、NH3·H2O是弱碱,部分电离,稀释10倍,促进电离,pH应是a-1<b<a,故错误;C、按照电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),故错误;D、依据越弱越水解,酸性:CH3COOH>H2CO3>HClO,因此水解程度:ClO->HCO3->CH3COO-,因此相同pH时,c(CH3COONa)>c(NaHCO3)>c(NaClO),因此c(Na+):①>②>③,故正确。
H++S2-,c(H+)>c(H2S),故错误;B、NH3·H2O是弱碱,部分电离,稀释10倍,促进电离,pH应是a-1<b<a,故错误;C、按照电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),故错误;D、依据越弱越水解,酸性:CH3COOH>H2CO3>HClO,因此水解程度:ClO->HCO3->CH3COO-,因此相同pH时,c(CH3COONa)>c(NaHCO3)>c(NaClO),因此c(Na+):①>②>③,故正确。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】以下元素均为短周期元素:
元素代号 | 相关信息 |
M | 非金属元素,其气态氢化物的水溶液呈碱性 |
A | A的单质与冷水剧烈反应,得到强碱性溶液 |
B | B的原子最外层电子数是内层电子数的三倍 |
C | 在第三周期中,C的简单离子半径最小 |
D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
E | 所有有机物中都含有E元素 |
(1)B在周期表中的位置______,C离子的结构示意图_______。
(2)D的最低价含氧酸的电子式______。
(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式____。(产物中无有毒有害物质)
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质。该反应的化学方程式:______。
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为 ___________。
【题目】用下图所示装置进行下列实验,实验结果与预测的现象不一致的是
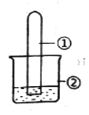
选项 | ①中的物质 | ②中的物质 | 预测装置中现象 |
A | NO2 | 蒸馏水 | 试管充满无色溶液 |
B | SO2 | 紫色石蕊溶液 | 溶液逐渐变为红色 |
C | NH3 | AlCl3溶液 | 产生白色沉淀 |
D | Cl2 | AgNO3溶液 | 产生白色沉淀 |
A. A B. B C. C D. D


