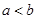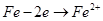题目内容
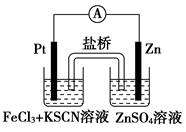
实验发现,298 K时,在 FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如右图所示的原电池装置。下列有关说法中正确的是( )

| A.该原电池的正极反应是:Zn-2e-=Zn2+ |
| B.左烧杯中溶液的红色逐渐褪去 |
| C.该电池铂电极上有气泡出现 |
| D.该电池总反应为:3Zn+2Fe3+=2Fe+3Zn2+ |
B
正极反应是得电子的反应,A错误;左烧杯中的电极反应式为Fe3++e-=Fe2+,B正确,C错误;因为在金属活动性顺序中铁排在H的前面,在酸性溶液中不会生成Fe,D错误。

练习册系列答案
相关题目

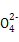 =2PbSO4+2H2O。下列有关说法正确的是( )
=2PbSO4+2H2O。下列有关说法正确的是( )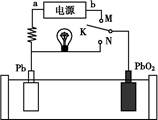

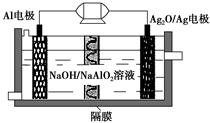

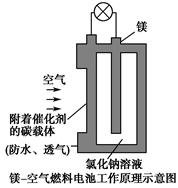
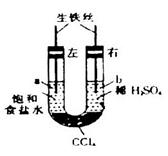
 ,分别在U形管两端小心倒入饱和食盐水和饱和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述错误的是
,分别在U形管两端小心倒入饱和食盐水和饱和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述错误的是