题目内容
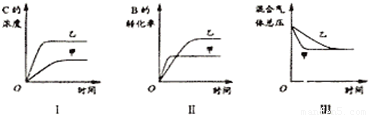
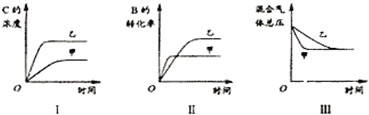
在容器固定的密闭容器中存在如下反应:A(g)+3B(g)?2C(g);△H<0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是( )

| A.图Ⅱ研究的是压强对反应的影响,且甲的压强较小 |
| B.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| C.图Ⅲ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| D.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
A、图Ⅱ根据到达平衡时间可知,如果甲、乙两个条件是压强对反应的影响,从化学反应速率来讲,是甲的压强较高,增大压强平衡向正反应移动,应该是甲条件下B的转化率比在乙条件下B的转化率高,与图象不符合,故A错误;
B、图I中,根据到达平衡时间可知,在乙条件下的化学反应速率,明显比在甲条件下的化学反应速率快;在乙条件下C的平衡浓度,比在甲条件下的C的平衡浓度大,相比较而言,条件乙既有利于此反应的化学反应速率增大又有利于平衡向正反应方向移动.说明甲、乙两个条件不仅影响化学反应速率,而且影响化学平衡,而催化剂不影响化学平衡故B错误;
C、催化剂只改变化学反应速率不影响化学平衡,但甲的时间短,反应速率快,则甲的催化效率高,故C错误;
D、温度高化学反应速率快,则甲的温度高,但是由于正反应放热,升高温度平衡左移,不利于反应向正反应方向进行,B的转化率减小,故D正确;
故选ABC.
B、图I中,根据到达平衡时间可知,在乙条件下的化学反应速率,明显比在甲条件下的化学反应速率快;在乙条件下C的平衡浓度,比在甲条件下的C的平衡浓度大,相比较而言,条件乙既有利于此反应的化学反应速率增大又有利于平衡向正反应方向移动.说明甲、乙两个条件不仅影响化学反应速率,而且影响化学平衡,而催化剂不影响化学平衡故B错误;
C、催化剂只改变化学反应速率不影响化学平衡,但甲的时间短,反应速率快,则甲的催化效率高,故C错误;
D、温度高化学反应速率快,则甲的温度高,但是由于正反应放热,升高温度平衡左移,不利于反应向正反应方向进行,B的转化率减小,故D正确;
故选ABC.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
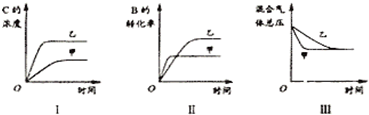
 a Z(g) + W(g) △H =-QkJ·mol-1 (Q>0)
a Z(g) + W(g) △H =-QkJ·mol-1 (Q>0)