题目内容
【题目】某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5mol/L的盐酸,右图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是
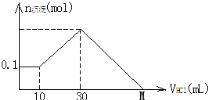
A. 70mL B. 130mL C. 120mL D. 100mL
【答案】B
【解析】
先分段分析图象,向所得浊液中,逐滴加入5mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:
①0~10mL,随盐酸的体积增加,生成沉淀的质量不变,则盐酸和氢氧化钠中和,说明该过程产生的沉淀是Mg(OH)2,n[Mg(OH)2]=0.1mol,NaOH、AlCl3、MgCl2组成的混合物,溶于足量水发生的反应是:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,NaOH有剩余,溶液是NaCl、NaAlO2和NaOH的混合液,该阶段发生反应是:NaOH+HCl=NaCl+H2O;
②10mL处,加入10mL盐酸刚好中和未反应的NaOH,溶液为NaCl、NaAlO2;
③10mL~30mL,随盐酸的体积增加,生成沉淀的质量增加,该阶段发生反应是NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;
④30mL处,NaAlO2与盐酸恰好反应,需盐酸体积为:30mL-10mL=20mL,沉淀质量达到最大,溶液为NaCl溶液;
⑤30mL~M点,随盐酸的体积增加,沉淀的质量减少,发生反应是:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O;
⑥M点,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液,结合方程式、原子守恒解答。
30mL时,溶液为NaCl溶液,溶液中Cl-来源于原混合物中的AlCl3、MgCl2和加入的30mLHCl,溶液中Na+来源于原混合物中的NaOH。
NaAlO2+HCl+H2O=Al(OH)3↓+NaCl
0.1mol 0.02L×5mol/L
由Al原子守恒得原混合物中n(AlCl3)=n(NaAlO2)=0.1mol
由Mg原子守恒得原混合物中n(MgCl2)=n[Mg(OH)2]=0.1mol,
由Na+离子和Cl-离子守恒得,原混合物中n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.1mol×2+0.1mol×3+0.03L×5mol/L=0.65mol。
M点溶液为MgCl2、AlCl3和NaCl混合液,M点所加盐酸相当于用于中和原混合物中的NaOH,此时所加盐酸物质的量:n(HCl)=n(NaOH)=0.65mol;M点所表示盐酸的体积为:V=0.65mol÷5mol/L=0.13L=130mL。答案选B。