题目内容
【题目】浓度均为![]() 的以下几种溶液:
的以下几种溶液:![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ,
,![]() 浓度由大到小的顺序是
浓度由大到小的顺序是![]()
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【答案】D
【解析】
浓度均为![]() 的以下几种溶液
的以下几种溶液![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ,先不考虑水解,
,先不考虑水解,![]() 、
、![]() 、
、![]() 都含有两个
都含有两个![]() ,所以它们
,所以它们![]() 的浓度大于其它4种物质,
的浓度大于其它4种物质,![]() 为弱电解质,其溶液中
为弱电解质,其溶液中![]() 小于铵盐的
小于铵盐的![]() ,再根据盐类的水解角度分析解答。
,再根据盐类的水解角度分析解答。
解:浓度均为![]() 的以下几种溶液
的以下几种溶液![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ;
;![]() ,
, ![]() 、
、![]() 、
、![]() 都含有两个
都含有两个![]() ,所以它们
,所以它们![]() 的浓度大于其它4种物质,而
的浓度大于其它4种物质,而![]() 中
中![]() 水解显酸性,
水解显酸性,![]() 水解显碱性,两者相互促进,所以
水解显碱性,两者相互促进,所以![]() 水解的量较多,
水解的量较多,![]() 的量较少;
的量较少;![]() 中亚铁离子水解呈酸性,抑制了
中亚铁离子水解呈酸性,抑制了![]() 水解,所以三种溶液中
水解,所以三种溶液中![]() :
:![]() ;
; ![]() 、
、![]() 、
、![]() 、
、![]() 中,
中,![]() 酸性最强,
酸性最强,![]() 水解受到的抑制最大,即
水解受到的抑制最大,即![]() 的量较多,溶液中
的量较多,溶液中![]() 较大;
较大;![]() ,溶液中
,溶液中![]() 小于铵盐的
小于铵盐的![]() ,应最小;
,应最小;![]() 溶液中
溶液中![]() 正常水解;
正常水解;![]() 溶液中,碳酸氢根离子水解呈碱性,促进了
溶液中,碳酸氢根离子水解呈碱性,促进了![]() 水解,其溶液中
水解,其溶液中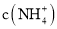 小于
小于![]() ,则溶液中
,则溶液中![]() :
:![]()
所以![]() 由大到小的顺序排列为:
由大到小的顺序排列为:![]() ,
,
故选:D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目