题目内容
【题目】甲胺(![]() )的性质与氨气相似,将pOH相同、体积均为
)的性质与氨气相似,将pOH相同、体积均为![]() 的CH3NH2H2O和
的CH3NH2H2O和![]() 两种溶液分别加水稀释至体积为V,pOH随
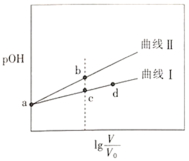
两种溶液分别加水稀释至体积为V,pOH随![]() 的变化关系如图所示,下列叙述错误的是( )
的变化关系如图所示,下列叙述错误的是( )
已知:常温下,![]() ,pOH=-lgc(OH-)。
,pOH=-lgc(OH-)。
A.稀释相同倍数时,CH3NH2H2O的浓度比![]() 的浓度大
的浓度大
B.溶液中水的电离程度:b点大于c点
C.由c点到d点,溶液中![]() 保持不变
保持不变
D.常温下,某盐酸的![]() ,a点时CH3NH2H2O的
,a点时CH3NH2H2O的![]() ,当
,当![]() 时,取等体积的两溶液混合,充分反应后:n(Cl-)>n(CH3NH3+)>n(H+)>n(OH-)
时,取等体积的两溶液混合,充分反应后:n(Cl-)>n(CH3NH3+)>n(H+)>n(OH-)
【答案】D
【解析】
甲胺(![]() )的性质与氨气相似,则CH3NH2H2O为弱碱。将pOH相同、体积均为
)的性质与氨气相似,则CH3NH2H2O为弱碱。将pOH相同、体积均为![]() 的CH3NH2H2O和
的CH3NH2H2O和![]() 两种溶液分别加水稀释至体积为V,从图中可以看出,稀释相同倍数时,曲线Ⅱ的pOH变化大,则曲线Ⅱ表示NaOH的pOH随
两种溶液分别加水稀释至体积为V,从图中可以看出,稀释相同倍数时,曲线Ⅱ的pOH变化大,则曲线Ⅱ表示NaOH的pOH随![]() 的变化,曲线Ⅰ表示CH3NH2H2O的pOH随
的变化,曲线Ⅰ表示CH3NH2H2O的pOH随![]() 的变化。
的变化。
A.由于CH3NH2H2O为弱碱,当CH3NH2H2O和![]() 的pOH相同时,CH3NH2H2O的浓度大,所以稀释相同倍数时,CH3NH2H2O的浓度比
的pOH相同时,CH3NH2H2O的浓度大,所以稀释相同倍数时,CH3NH2H2O的浓度比![]() 的浓度大,A正确;
的浓度大,A正确;
B.溶液中pOH b点大于c点,则c点溶液中c(OH-)大,对水电离的抑制作用大,所以溶液中水的电离程度:b点大于c点,B正确;
C.溶液中![]() =
=![]() =
=![]() ,由c点到d点,溶液的温度不变,KW、Kb不变,所以保持不变,C正确;
,由c点到d点,溶液的温度不变,KW、Kb不变,所以保持不变,C正确;
D.常温下,当![]() 时,盐酸溶液中的c(H+)与CH3NH2H2O溶液中c(OH-)相等,取等体积的两溶液混合,则反应生成CH3NH3Cl,同时CH3NH2H2O有剩余,CH3NH2H2O继续发生电离而使溶液显碱性,从而得出n(CH3NH3+) n(Cl-)>n(OH-)>n(H+),D错误;
时,盐酸溶液中的c(H+)与CH3NH2H2O溶液中c(OH-)相等,取等体积的两溶液混合,则反应生成CH3NH3Cl,同时CH3NH2H2O有剩余,CH3NH2H2O继续发生电离而使溶液显碱性,从而得出n(CH3NH3+) n(Cl-)>n(OH-)>n(H+),D错误;
故选D。

【题目】在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(X) | n(Y) | n(M) | |||
① | 700 | 0.40 | 0.10 | 0.090 | |
② | 800 | 0.10 | 0.40 | 0.080 | |
③ | 800 | 0.20 | 0.30 | a | |
④ | 900 | 0.10 | 0.15 | b | |
下列说法正确的是( )
A. 实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B. 实验②中,该反应的平衡常数K=2.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.060