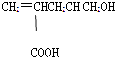题目内容
【题目】某混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL该溶液进行如下实验:
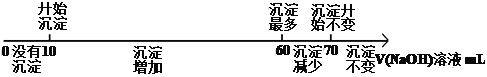
①第一份加入AgNO3溶液有沉淀产生。
②第二份加足量NaOH溶液加热后,收集到气体0.04mol。
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验数据,填写下列空白。
(1)一定不存在的离子有___________________。
(2)第②步操作发生反应的离子方程式为_________________________。
(3)第③步操作确定的离子有____________________________。
(4)对无法确定是否存在的离子,满足___________________时,能确定其存在。
【答案】 Mg2+、Ba2+ NH4++OH-![]() NH3↑+ H2O CO32-、SO42- K+物质的量>0.02mol
NH3↑+ H2O CO32-、SO42- K+物质的量>0.02mol
【解析】①第一份加入AgNO3溶液有沉淀产生,不能说明溶液中存在Cl-;②第二份加足量NaOH溶液加热后产生0.04mol为氨气,溶液中一定含有NH4+,并且物质的量为0.04mol;③不溶于盐酸的2.33g为硫酸钡,物质的量是0.01mol;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g-2.33g=3.94g,碳酸钡的物质的量为0.02mol,故一定存在CO32-、SO42-,因而一定没有Mg2+、Ba2+;根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;n(-)=2n(CO32-)+2n(SO42-)=0.06mol,故一定有K+,至少0.02mol;
(1)根据以上分析可知一定不存在的离子有Mg2+、Ba2+。(2)第②步操作发生反应的离子方程式为NH4++OH-![]() NH3↑+H2O。(3)第③步操作确定的离子有CO32-、SO42-。(4)氯离子不能确定,根据电荷守恒可知只要满足K+物质的量>0.02mol时,能确定氯离子存在。
NH3↑+H2O。(3)第③步操作确定的离子有CO32-、SO42-。(4)氯离子不能确定,根据电荷守恒可知只要满足K+物质的量>0.02mol时,能确定氯离子存在。

【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且30分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中的溶液从色变为色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察;
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 , 由此造成的测定结果(填偏高、偏低或无影响);
(4)步骤②缺少的操作是;
(5)如图,是某次滴定时的滴定管中的液面,其读数为mL;
(6)根据如表数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度为mol/L.
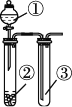
【题目】利用如图所示装置进行下列实验,能达到实验目的的是 ( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | 铜 | 溴水 | 验证浓硫酸具有强氧化性 | |
B | 浓盐酸 | 浓硫酸 | 空气 | 制取并收集HCl | |
C | 浓氨水 | 氧化钙 | 空气 | 制取并收集NH3 | |
D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 验证酸性:硫酸>碳酸>硅酸 |
A. A B. B C. C D. D