题目内容
若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应中化合价发生变化和未发生变化的N原子数之比为( )
| A.1?:4 | B.1?:2 |
| C.2?:1 | D.4?:1 |
B
根据反应物、生成物及电子守恒配平反应方程式为:3(NH4)2SO4===3SO2↑+N2↑+4NH3↑+6H2O,生成N2中的N原子化合价升高,生成NH3中的N原子化合价反应前后未变,二者个数之比为1?:2。

练习册系列答案
相关题目


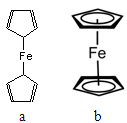
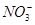 、Fe3+、
、Fe3+、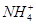 、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是