题目内容
 (Ⅰ)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
(Ⅰ)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).(1)丙烷脱氢可得丙烯.
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ/mol
CH3CH═CH2(g)CH4(g)+HC≡CH(g)△H2=+32.4kJ/mol
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的△H=
(2)以丙烷为燃料制作新型燃料电池,电池的一极通入O2和CO2,另一极通入丙烷,电解质是熔融碳酸盐.通丙烷的一极是电池的
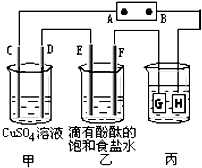
(Ⅱ)如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和物质的量浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
(1)A极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
(4)图甲装置电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则乙装置中,若不考虑Cl2的溶解及与碱的反应,此装置共产生气体
分析:Ⅰ、(1)依据热化学方程式和盖斯定律计算得到;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,以此来书写电池总反应方程式,原电池中阴离子向负极移动;
Ⅱ、(1)将直流电源接通后,F极附近呈红色,可知道氢离子在该电极放电,所以F即是阴极,并得到其他各个电极的名称;
(2)C、D、E、F电极转移的电子数目相等,根据转移电子数可计算生成的单质的量;
(3)电镀装置中,镀层金属必须做阳极,镀件做阴极,各个电极上转移的电子数是相等的;
(4)依据电解池中电极反应和电子守恒分析计算.
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,以此来书写电池总反应方程式,原电池中阴离子向负极移动;
Ⅱ、(1)将直流电源接通后,F极附近呈红色,可知道氢离子在该电极放电,所以F即是阴极,并得到其他各个电极的名称;
(2)C、D、E、F电极转移的电子数目相等,根据转移电子数可计算生成的单质的量;
(3)电镀装置中,镀层金属必须做阳极,镀件做阴极,各个电极上转移的电子数是相等的;
(4)依据电解池中电极反应和电子守恒分析计算.
解答:解:(1)由C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ?mol-1①,
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ?mol-1 ②,
则根据盖斯定律,反应C3H8(g)→CH3CH=CH2(g)+H2(g)可由①-②得到,
所以△H=△H1-△H2=+156.6kJ?mol-1-(+32.4kJ?mol-1)=+124.2kJ?mol-1,故答案为:+124.2;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,即丙烷与氧气反应生成二氧化碳和水,则电池的总反应为C3H8+5O2═3CO2+4H2O,负极电极反应为:C3H8+10CO32--20e-═4H2O+13CO2,原电池中阴离子向负极移动,即CO32-移向电池的负极,
故答案为:负,C3H8+10CO32--20e-═4H2O+13CO2;负;
Ⅱ、将直流电源接通后,F极附近呈红色,说明F极显碱性,是氢离子在该电极放电,所以F即是阴极,可得出D、F、H、Y均为阴极,C、E、G、X均为阳极,A是电源的正极,B是负极;
(1)B电极是电源的负极,A是电源的正极;
故答案为:正;
(2)C、D、E、F电极发生的电极反应分别为:4OH-═O2↑+2H2O+4e-、Cu2++2e-═Cu、2Cl-═Cl2↑+2e-、2H++2e-═H2↑,当各电极转移电子均为1mol时,生成单质的量分别为:0.25mol、0.5mol、0.5mol、0.5mol,所以单质的物质的量之比为1:2:2:2;
故答案为:1:2:2:2;
(3)电镀装置中,镀层金属必须做阳极,镀件做阴极,所以H应该是镀件,电解质溶液为硝酸银溶液;当乙中溶液的c(OH-)=0.1mol/L(此时乙溶液体积为500mL)时,根据电极反应2H++2e-═H2↑,则放电的氢离子的物质的量为:0.1mol/l×0.5L=0.05mol,当转移0.05mol电子时,丙中镀件上析出银的质量=108g/mol×0.05mol=5.4g,电解硫酸铜的过程中氢氧根减少,所以氢离子浓度增大,所以酸性增强,甲中溶液的氢离子浓度变大,故答案为:镀件;硝酸银;5.4g;变大;
(4)图甲装置电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则乙装置中,若不考虑Cl2的溶解及与碱的反应,甲装置的电解方程式为:2CuSO4+2H2O
2H2SO4+2Cu+O2↑,乙中电解饱和食盐水发生的离子方程式为2Cl-+2H2O
2OH-+H2↑+Cl2↑;
甲池溶液通电一段时间后,向所得的溶液中加入0.2mol的Cu(OH)2后恰好恢复到电解前的浓度,发生2CuSO4+2H2O
2Cu+O2↑+2H2SO4、2H2O
2H2↑+O2↑,由Cu(OH)2
CuO+H2O,则转移的电子数为(0.2mol×2+0.2mol×2)×NA=0.8NA,物质的量为0.8mol,依据电子守恒,主要2mol电子生成1mol氢气和1mol氯气,乙装置共产生气体物质的量共0,8mol,标准状况体积=0.8mol×22.4L/mol=17.92L,
故答案为:17.92.
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ?mol-1 ②,
则根据盖斯定律,反应C3H8(g)→CH3CH=CH2(g)+H2(g)可由①-②得到,
所以△H=△H1-△H2=+156.6kJ?mol-1-(+32.4kJ?mol-1)=+124.2kJ?mol-1,故答案为:+124.2;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,即丙烷与氧气反应生成二氧化碳和水,则电池的总反应为C3H8+5O2═3CO2+4H2O,负极电极反应为:C3H8+10CO32--20e-═4H2O+13CO2,原电池中阴离子向负极移动,即CO32-移向电池的负极,
故答案为:负,C3H8+10CO32--20e-═4H2O+13CO2;负;
Ⅱ、将直流电源接通后,F极附近呈红色,说明F极显碱性,是氢离子在该电极放电,所以F即是阴极,可得出D、F、H、Y均为阴极,C、E、G、X均为阳极,A是电源的正极,B是负极;
(1)B电极是电源的负极,A是电源的正极;
故答案为:正;
(2)C、D、E、F电极发生的电极反应分别为:4OH-═O2↑+2H2O+4e-、Cu2++2e-═Cu、2Cl-═Cl2↑+2e-、2H++2e-═H2↑,当各电极转移电子均为1mol时,生成单质的量分别为:0.25mol、0.5mol、0.5mol、0.5mol,所以单质的物质的量之比为1:2:2:2;
故答案为:1:2:2:2;
(3)电镀装置中,镀层金属必须做阳极,镀件做阴极,所以H应该是镀件,电解质溶液为硝酸银溶液;当乙中溶液的c(OH-)=0.1mol/L(此时乙溶液体积为500mL)时,根据电极反应2H++2e-═H2↑,则放电的氢离子的物质的量为:0.1mol/l×0.5L=0.05mol,当转移0.05mol电子时,丙中镀件上析出银的质量=108g/mol×0.05mol=5.4g,电解硫酸铜的过程中氢氧根减少,所以氢离子浓度增大,所以酸性增强,甲中溶液的氢离子浓度变大,故答案为:镀件;硝酸银;5.4g;变大;
(4)图甲装置电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则乙装置中,若不考虑Cl2的溶解及与碱的反应,甲装置的电解方程式为:2CuSO4+2H2O
| ||
| ||
甲池溶液通电一段时间后,向所得的溶液中加入0.2mol的Cu(OH)2后恰好恢复到电解前的浓度,发生2CuSO4+2H2O
| ||
| ||
| ||
故答案为:17.92.
点评:本题考查学生有关电解池的工作原理知识,综合性很强,难度较大,要求学生熟记教材知识,学以致用,明确原原电池和电解池的工作原理是解题关键,难度中等.

练习册系列答案
相关题目
 HCO3-+H+的平衡常数K1=
HCO3-+H+的平衡常数K1= CO32-+H+,HCO3-+H2O
CO32-+H+,HCO3-+H2O H2CO3+OH-,
H2CO3+OH-,