ЬтФПФкШн
ЁОЬтФПЁП(1)РћгУЗДгІCuЃЋ2FeCl3=CuCl2ЃЋ2FeCl2ЩшМЦГЩШчЭМЫљЪОдЕчГиЃЌЛиД№ЯТСаЮЪЬтЃК
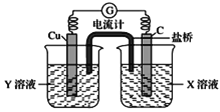
ЂйаДГіЕчМЋЗДгІЪНЃКе§МЋ__________________________ ЃЛ
ЂкЭМжаXШмвКЪЧ_______________ЃЌ
ЂлдЕчГиЙЄзїЪБЃЌбЮЧХжаЕФ________(ЬюЁАбєЁБЛђЁАвѕЁБ)РызгЯђXШмвКЗНЯђвЦЖЏЁЃ
(2)ШчЭМЪЧвЛИіЛЏбЇЙ§ГЬЕФЪОвтЭМЁЃ
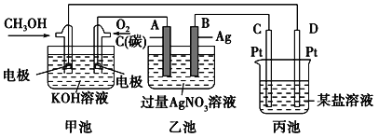
ЂйМзГижаOH-вЦЯђ__________МЋЃЈЬюЁАCH3OHЁБЛђЁАO2ЁБЃЉЁЃ
ЂкаДГіЭЈШыCH3OHЕФЕчМЋЕФЕчМЋЗДгІЪН_______________ЁЃ
ЂлввГижазмЗДгІЕФРызгЗНГЬЪН___________________ЁЃ
ЂмЕБввГижаBЃЈA gЃЉМЋЕФжЪСПдіМг5.40gЃЌШєДЫЪБввГижаШмвКЕФЬхЛ§ЮЊ500mlЃЌдђШмвКЕФC(H+)ЪЧ___________ЃЛДЫЪББћГиФГЕчМЋЮіГі1.60gФГН№ЪєЃЌдђБћжаЕФФГбЮШмвКПЩФмЪЧ______________ЃЈЬюађКХЃЉЁЃAЃЎMgSO4 BЃЎCuSO4 CЃЎNaCl DЃЎAgNO3
ЁОД№АИЁПFe3ЃЋЃЋe-=Fe2ЃЋ FeCl3 бє CH3OH CH3OH-6e-+8OH-=CO32-+6H2O 4Ag++2H2O![]() 4Ag+O2Ёќ+4H+ 0.1molЁЄLЃ1 BD
4Ag+O2Ёќ+4H+ 0.1molЁЄLЃ1 BD
ЁОНтЮіЁП
(1) ЂйЗДгІCuЃЋ2FeCl3=CuCl2ЃЋ2FeCl2жаЃЌЭЪЇЕчзгЗЂЩњбѕЛЏЗДгІЃЌFe3+ЕУЕчзгЗЂЩњЛЙдЗДгІЃЌдЕчГижае§МЋЗЂЩњЛЙдЗДгІЃЌЬМзіе§МЋЃЌЗЂЩњЕФЛЙдЗДгІЮЊЃКFe3ЃЋЃЋe-=Fe2ЃЋЃЛзлЩЯЫљЪіЃЌБОЬтД№АИЪЧЃКFe3ЃЋЃЋe-=Fe2ЃЋЁЃ
ЂкЪЏФЋЪЧе§МЋЃЌе§МЋМЋЗДгІЮЊЃКFe3ЃЋЃЋe-=Fe2ЃЋЃЌЫљвдЭМжаXШмвКЪЧFeCl3 ШмвКЃЛзлЩЯЫљЪіЃЌБОЬтД№АИЪЧЃКFeCl3 ЁЃ
ЂлдЕчГиЙЄзїЪБЃЌбєРызгвЦЯђе§МЋЃЌЪЏФЋЪЧе§МЋЃЌЫљвдбЮЧХжаЕФбєРызгЯђXШмвКЗНЯђвЦЖЏЃЛзлЩЯЫљЪіЃЌБОЬтД№АИЪЧЃКбєЁЃ
(2) ЂйШМСЯЕчГижа,ЭЖЗХШМСЯЕФЕчМЋЪЧИКМЋ,ЭЖЗХбѕЛЏМСЕФЕчМЋЪЧе§МЋ,дЕчГиЗХЕчЪБ,ЕчНтжЪШмвКжаЧтбѕИљРызгЯђИКМЋвЦЖЏ,МДЯђЭЖЗХМзДМЕФЕчМЋвЦЖЏЃЛзлЩЯЫљЪіЃЌБОЬтД№АИЪЧЃКCH3OHЁЃ
ЂкИУШМСЯЕчГижа,МзДМЪЇЕчзгКЭЧтбѕИљРызгЗДгІЩњГЩЬМЫсИљРызгКЭЫЎ,ЕчМЋЗДгІЪНЮЊ: CH3OH-6e-+8OH-=CO32-+6H2OЃЛвђДЫЃЌБОЬте§ШЗД№АИЪЧЃКCH3OH-6e-+8OH-=CO32-+6H2OЁЃ
ЂлЕчНтЯѕЫсвјШмвКЪБ,вјРызгЕУЕчзгЩњГЩвјЁЂЫЎЪЇЕчзгЩњГЩбѕЦјКЭЧтРызг,РызгЗНГЬЪНЮЊ4Ag++2H2O![]() 4Ag+O2Ёќ+4H+ ЃЛзлЩЯЫљЪіЃЌБОЬтД№АИЪЧЃК4Ag++2H2O
4Ag+O2Ёќ+4H+ ЃЛзлЩЯЫљЪіЃЌБОЬтД№АИЪЧЃК4Ag++2H2O![]() 4Ag+O2Ёќ+4H+ЁЃ
4Ag+O2Ёќ+4H+ЁЃ
ЂмЕБввГижаBЃЈAgЃЉМЋЕФжЪСПдіМг5.40g ЪБЃЌЩшЧтРызгХЈЖШЮЊxmol/LЃЌ4Ag++2H2O![]() 4Ag+O2Ёќ+4H+ЃЌИљОнЗДгІЙиЯЕЃК4Ag---4H+ЃЌ432ЃК4=5.4ЃК0.5xЃЌМЦЫуЕУГі: x=0.1ЃЌЫљвдШмвКЕФc(H+)=0.1molЁЄLЃ1ЃЛвѕМЋЩЯЮіГіН№ЪєЃЌдђдкН№ЪєЛюЖЏадЫГађБэжаН№ЪєдЊЫиДІгкHдЊЫиКѓЃЌИљОнДЎСЊЕчГижазЊвЦЕчзгЪ§ЯрЕШжЊЃЌБћжаЮіГіН№ЪєдЊЫиашвЊЕФЕчзгЕШгкЛђаЁгкввГижазЊвЦЕчзгЪ§ЃЌОнДЫШЗЖЈКЌгаЕФН№ЪєдЊЫи,ЮіГі5.40g ЪБзЊвЦЕчзгЪЧ0.05molЃЛДЫЪББћГиФГЕчМЋЮіГі1.60gФГН№ЪєЃЌдђБћжаЕФФГбЮШмвКПЩФмЪЧЃК
4Ag+O2Ёќ+4H+ЃЌИљОнЗДгІЙиЯЕЃК4Ag---4H+ЃЌ432ЃК4=5.4ЃК0.5xЃЌМЦЫуЕУГі: x=0.1ЃЌЫљвдШмвКЕФc(H+)=0.1molЁЄLЃ1ЃЛвѕМЋЩЯЮіГіН№ЪєЃЌдђдкН№ЪєЛюЖЏадЫГађБэжаН№ЪєдЊЫиДІгкHдЊЫиКѓЃЌИљОнДЎСЊЕчГижазЊвЦЕчзгЪ§ЯрЕШжЊЃЌБћжаЮіГіН№ЪєдЊЫиашвЊЕФЕчзгЕШгкЛђаЁгкввГижазЊвЦЕчзгЪ§ЃЌОнДЫШЗЖЈКЌгаЕФН№ЪєдЊЫи,ЮіГі5.40g ЪБзЊвЦЕчзгЪЧ0.05molЃЛДЫЪББћГиФГЕчМЋЮіГі1.60gФГН№ЪєЃЌдђБћжаЕФФГбЮШмвКПЩФмЪЧЃК
AЁЂСђЫсУОжаУОдЊЫиДІгкHдЊЫиЧА,ЫљвдвѕМЋЩЯВЛЮіГіН№ЪєЕЅжЪЃЌЙЪДэЮѓЃЛ
BЁЂЕчНтСђЫсЭШмвКЪБ,вѕМЋЩЯЮіГі1.6gЭашвЊзЊвЦЕчзг0.05mol,ЙЪе§ШЗЃЛ
CЁЂNaClжаФЦдЊЫиДІгкЧтдЊЫиЧАЃЌЫљвдвѕМЋЩЯВЛЮіГіН№ЪєЕЅжЪЃЌЙЪДэЮѓЃЛ
DЁЂЕчНтЯѕЫсвјШмвКЪБ,вѕМЋЩЯЮіГі1.6g вјашвЊзЊвЦЕчзг0.0148mol<0.05mol,ЙЪе§ШЗЃЛ
вђДЫЃЌБОЬтбЁ:BDЁЃ
злЩЯЫљЪіЃЌБОЬтД№АИЪЧЃК0.1molЁЄLЃ1ЃЛBDЁЃ

 дѕбљбЇКУХЃНђгЂгяЯЕСаД№АИ
дѕбљбЇКУХЃНђгЂгяЯЕСаД№АИЁОЬтФПЁПХ№(B)ПЩаЮГЩH3BO3ЁЂNaBH4ЁЂNaBO2ЕШЛЏКЯЮяЃЌгУЭОЙуЗКЁЃ
(1)H3BO3ЮЊвЛдЊШѕЫсЃЌГЃЮТЯТЃЌдкЫЎжаДцдкШчЯТЕчРыЦНКтЃКH3BO3 + H2O![]() [B(OH)4]-+H+ЃЌKa=5.72ЁС10-10ЁЃ
[B(OH)4]-+H+ЃЌKa=5.72ЁС10-10ЁЃ
Ђй25ЁцЪБЃЌ0.175 mol/LЕФH3BO3ШмвКpHдМЮЊ_________ЁЃ
ЂквбжЊЬМЫсH2CO3ЕФЕчРыЦНКтГЃЪ§ЮЊKa1 = 4.4ЁС10-7ЃЌKa2 = 4.7ЁС10-11ЁЃНЋЩйСПЬМЫсФЦШмвКЕЮМгЕНБЅКЭХ№ЫсШмвКжаЃЌЗДгІЕФРызгЗНГЬЪНЮЊ_________ЁЃ
(2)дкШнЛ§КуЖЈЮЊ2 LЕФУмБеШнЦїжаМгШызуСПBPO4КЭNaЙЬЬхВЂГфШывЛЖЈСПЕФH2(g)ЗЂЩњДЂЧтЗДгІЃКBPO4(s)+4Na(s)+2H2(g)![]() Na3PO4(s)+NaBH4(s) ЁїHЃМ0
Na3PO4(s)+NaBH4(s) ЁїHЃМ0
ЂйЬхЯЕжаH2ЕФЮяжЪЕФСПгыЗДгІЪБМфЕФЙиЯЕШчБэЫљЪОЃК
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
n(H2)/mol | 2.0 | 1.5 | 1.2 | 0.9 | 0.8 | 0.8 |
ЯТСагаЙиа№Ъіе§ШЗЕФЪЧ(ЬюБъКХ)_________ЁЃ
a. ЕБШнЦїФкЦјЬхЕФФІЖћжЪСПВЛдйБфЛЏЪБЃЌЗДгІДяЕНЦНКтзДЬЌ
b. 10 minЪБЯђШнЦїФкЭЈШыЩйСПH2ЃЌдђжиаТДяЦНКтЧАІЭ(ЗХЧт)> ІЭ(ЮќЧт)
c. БЃГжЮТЖШВЛБфЃЌЦНКтКѓдйГфШы1 mol H2ЃЌДяаТЦНКтЪБH2ЕФХЈЖШЮЊ0.4 mol/L
d. Щ§ИпЮТЖШЃЌЗХЧтЫйТЪМгПьЃЌжиаТДяЕНЦНКтЪБШнЦїбЙЧПдіДѓ
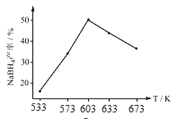
ЂкЭМЮЊВњТЪгыЗДгІЮТЖШЕФЙиЯЕЧњЯпЃЌNaBH4ЕФВњТЪдк603KжЎЧАЫцЮТЖШЩ§ИпЖјдіДѓЃЌдк603KжЎКѓЫцЮТЖШЩ§ИпЖјМѕаЁЕФдвђЪЧ_________ЁЃ
(3)NaBH4(s)гіH2O(l)ОчСвЫЎНтЃЌЩњГЩЧтЦјКЭNaBO2(s)ЁЃ
ЂйЭЈГЃзДПіЯТЃЌЪЕбщВтЕУ3.8 g NaBH4(s)ЗЂЩњЫЎНтЗДгІЗХГі21.6 kJШШСПЃЌаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН_________ЁЃ
Ђк![]() ЮЊNaBH4ЫЎНтЕФАыЫЅЦк(ЫЎНтвЛАыЫљашвЊЕФЪБМфЃЌЕЅЮЛЮЊmin)ЁЃlg
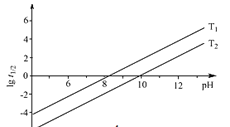
ЮЊNaBH4ЫЎНтЕФАыЫЅЦк(ЫЎНтвЛАыЫљашвЊЕФЪБМфЃЌЕЅЮЛЮЊmin)ЁЃlg![]() ЫцpHКЭЮТЖШЕФБфЛЏШчЭМЫљЪОЁЃШмвКpH=4ЪБЃЌNaBH4_________(ЬюЁАФмЁБЛђЁАВЛФмЁБ)ЮШЖЈДцдкЃЌдвђЪЧ_________(гУРызгЗНГЬЪНБэЪО)ЃЛT1_________T2ЁЃ(Ью ЁА>ЁБЛђЁА<ЁБ)
ЫцpHКЭЮТЖШЕФБфЛЏШчЭМЫљЪОЁЃШмвКpH=4ЪБЃЌNaBH4_________(ЬюЁАФмЁБЛђЁАВЛФмЁБ)ЮШЖЈДцдкЃЌдвђЪЧ_________(гУРызгЗНГЬЪНБэЪО)ЃЛT1_________T2ЁЃ(Ью ЁА>ЁБЛђЁА<ЁБ)
ЂлХ№ЧтЛЏФЦОпгаМЋЧПЛЙдадЃЌМюадЬѕМўПЩгУгкДІРэЕчЖЦЗЯвКжаЕФCuSO4жЦЕУФЩУзЭЃЌДгЖјБфЗЯЮЊБІЁЃаДГіЕчЖЦбєМЋЗДгІЗНГЬЪН_______________ЁЃ
ЁОЬтФПЁПввЯЉЪЧживЊЕФЛљБОЛЏЙЄдСЯЃЌвдввЭщЮЊдСЯЩњВњввЯЉгаЖржжЗНЗЈЁЃ
I.ввЭщСбНтЭбЧтЗЈЁЃИУЗНЗЈЕФЗДгІЮЊЃКC2H6(g)=C2H4(g)+H2(g) ЁїH=akJ/mol
(1)вбжЊ101kPaЃЌ298KЪБЃЌC(s)КЭH2(g)ЩњГЩlmoC2H6(g)ЁЂ1molC2H4(g)ЕФЁїHЗжБ№ЮЊЃ84.7 kJ/molЁЂ+52.3kJ/molЁЃдђa=___________ЁЃ
II.ввЭщбѕЛЏЭбЧтЗЈЃЌдкдСЯЦјжаМгШыбѕЦјЃЌввЭщбѕЛЏЭбЧтЕФЗДгІШчЯТЃК2C2H6(g)+O2(g)![]() 2C2H4(g)+2H2O(g) ЁїH<0ЃЌИБЗДгІЖМЮЊЗХШШЗДгІЃЌИБВњЮягаCH4(g)ЁЂCO(g)ЁЂCO2(g)ЁЃдСЯЦј(70.1%ПеЦјЁЂ29.9%C2H6)дкЗДгІЦїжаЭЃСє15sЃЌЛёЕУЯрЙиЪ§ОнШчЯТБэЃК
2C2H4(g)+2H2O(g) ЁїH<0ЃЌИБЗДгІЖМЮЊЗХШШЗДгІЃЌИБВњЮягаCH4(g)ЁЂCO(g)ЁЂCO2(g)ЁЃдСЯЦј(70.1%ПеЦјЁЂ29.9%C2H6)дкЗДгІЦїжаЭЃСє15sЃЌЛёЕУЯрЙиЪ§ОнШчЯТБэЃК
ЗДгІЮТЖШ/Ёц | ввЭщзЊЛЏТЪ/% | ввЯЉбЁдёад/% | ВњТЪ/% |
750 | 80.5 | 62.9 | 50.6 |
800 | 85.6 | 64.5 | 55.2 |
850 | 92.2 | 63.2 | 58.3 |
900 | 97.6 | 59.0 | 57.6 |
(2)ЂйЗДгІЕФЦНКтГЃЪ§БэДяЪНЮЊK=___________ЃЌK(750Ёц)___________K(900Ёц)(ЬюЁА>ЁБЁЂЁА<ЁБЁЂЁА=ЁБ)
ЂкЕБЮТЖШГЌЙ§800ЁцЪБЃЌввЯЉЕФбЁдёадНЕЕЭЃЌЦфжївЊдвђПЩФмЪЧ________________ЁЃ
III.ДпЛЏбѕЛЏЭбЧтЗЈЁЃвдMo-V-Nb-SbЕФбѕЛЏЮяЮЊДпЛЏМСЃЌдкГЃбЙЁЂ380ЁцЯТЃЌЗДгІЫйТЪгыбѕЦјЗжбЙ[P(O2)]ЁЂввЭщЗжбЙ[P(C2H6)ЕФЙиЯЕШчЯТЭМЫљЪОЁЃ
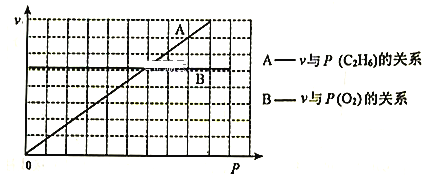
(3)вбжЊИУЗДгІЕФЫйТЪЗНГЬЮЊv=kPm(O2)ЁЄPn(C2H6)ЃЌдђm=___________ЃЌn=___________ЁЃ
IVжЪзгФЄШМСЯЕчГиЗЈЁЃ
(4)ввЭщбѕЛЏжЦввЯЉЛсВњЩњCO2ЕФДѓСПХХЗХЃЌНќФъбаОПШЫдБПЊЗЂСЫввЭщбѕЛЏжЦввЯЉЕФжЪзгФЄШМСЯЕчГи(SOFC)ЃЌИУШМСЯЕчГиЕФИКМЋЗДгІЪНЮЊ__________ЃЌетжжЕчГиЙЄзїЙ§ГЬжаУЛгаCO2ХХЗХЃЌдвђЪЧ______________ЁЃ