题目内容
Ⅰ.Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
请回答下列问题:
(1)电池的负极材料为 ,电解液中Li+的移动方向是由 极到
极(填“正”或“负”)。
(2)电池正极发生的电极反应为 。
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 。
(4)组装该电池必须在无水、无氧的条件下进行,原因是
。
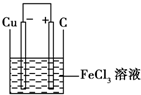
Ⅱ.某地区的酸雨情况严重,钢铁锈蚀非常明显,其腐蚀属于电化学腐蚀中的______腐蚀;右图为该地区钢铁腐蚀原理的简图,正极的电极反应式为 。该图某处稍作修改即可成为钢铁电化学防护的简单示意图,请画出修改后的简单示意图,并标出电子流动方向。
(1)锂(或Li)(1分) 负,正(2分) (2)![]() (3分)
(3分)
(3)出现白雾,有刺激性气体生成 (2分) ![]() (2分)
(2分)
(4)锂是活泼金属,易与![]() 、
、![]() 反应;
反应;![]() 也可与水反应(2分)
也可与水反应(2分)
(5)析氢(1分),2H+ + 2e-= H2↑ (1分)
解析:略

| A、锂电极发生还原反应 | B、电子通过外电路从锂电极流向碳电极 | C、每生成1mol SO2转移4mol电子 | D、SOCl2既是氧化剂又是还原剂 |
 (Ⅰ)原电池是一种将
(Ⅰ)原电池是一种将