题目内容
【题目】下列各项表述与示意图形不一致的是

A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液pH随加酸体积的变化
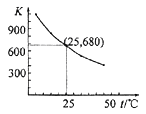
B. 图②中曲线表示反应2SO2(g) + O2(g)![]() 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量0.1 mol·L-1草酸溶液混合,n(Mn2+) 随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g)+ H2(g) →CH3CH3(g);ΔH>0使用和未使用催化剂时,反应过程中的能量变化
【答案】A
【解析】试题分析:A.用盐酸滴定氢氧化钠溶液,当恰好中和时溶液的pH=7,酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,题中图象变化与实际不相符,故A错误;B.因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K(逆)会增大,而K(正)会减小,图象中变化与实际上的变化相符,故B正确;C.该反应是放热反应,反应生成的Mn2+对该反应有催化作用,故反应速率越来越快,不是恒定速率,故C错误;D.图象a活化能减小,a使用了催化剂,因该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是吸热反应,故D错误;答案为B。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案【题目】Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(1)R的元素符号为_______; M在元素周期表中的位置为___________________。
(2)X与Y按原子个数比1:1构成的物质的电子式为________;所含化学键类型________。
(3)X+, Y2,M2 离子半径大小顺序为________________________________。
(4)将YM2通入FeCl3溶液中的离子方程式_________________________________。
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式___________________________________________________________。
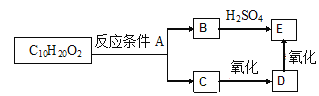
Ⅱ.如下图转化关系
![]()
①若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________。
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为_______________________________________________________________________________。