��Ŀ����
����Ŀ�� H2O2��һ����ɫ�Լ����ڻ�ѧ��ҵ�����������������ᡢ�������Ƶȵ�ԭ�ϣ�ҽҩ��ҵ����ɱ������������.ij��ѧС����̽��˫��ˮ��������������ʵ�飺
(1)�±��Ǹ�С���о�Ӱ���������(H2O2)�ֽ����ʵ�����ʱ�ɼ���һ�����ݣ���![]() ��ȡ
��ȡ![]() �����ʱ��
�����ʱ��![]() ��
��![]()
Ũ�� ʱ�� ��Ӧ���� |
|
|
|
|
������������ | ��������Ӧ | ��������Ӧ | ��������Ӧ | ��������Ӧ |
���������� | 360 | 480 | 540 | 720 |
| 10 | 25 | 60 | 120 |
���о�С������Ʒ���ʱ��������Ũ�ȡ� ______ �� ______ ���ضԹ�������ֽ����ʵ�Ӱ�졣(2)��һ�о�С������ͬŨ��Fe3+�Ĵ��£�̽��H2O2Ũ�ȶ�H2O2�ֽⷴӦ���ʵ�Ӱ�죬��ѡ�Լ�������![]() ��
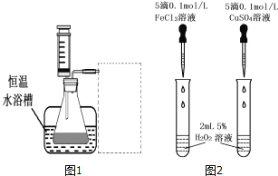
��![]() ������ˮ����ƿ��˫������ˮ�ۡ����ܡ��������ܡ���Ͳ�����������ˮԡ�ۡ�ע���������ʵ��װ�ã����ͼ1�����ڵ�װ��ʾ��ͼ
������ˮ����ƿ��˫������ˮ�ۡ����ܡ��������ܡ���Ͳ�����������ˮԡ�ۡ�ע���������ʵ��װ�ã����ͼ1�����ڵ�װ��ʾ��ͼ![]() Ҫ������õ�������ֱ�����ַ�Ӧ���ʴ�С_________
Ҫ������õ�������ֱ�����ַ�Ӧ���ʴ�С_________
(3)����H2O2�ֽⷴӦ��![]() Ҳ��һ���Ĵ����á�Ϊ�Ƚ�Fe3+��
Ҳ��һ���Ĵ����á�Ϊ�Ƚ�Fe3+��![]() ��H2O2�ֽ�Ĵ�Ч�����о�С���ͬѧ�������ͼ2��ʾ��ʵ�顣��ش�������⣺
��H2O2�ֽ�Ĵ�Ч�����о�С���ͬѧ�������ͼ2��ʾ��ʵ�顣��ش�������⣺
�ٿ�ͨ���۲� ____________ ���Ƚϵó����ۡ�
����ͬѧ�����![]() ��
��![]() ��Һ��Ϊ
��Һ��Ϊ![]() ��Ϊ�������������� _________ ��
���������������� _________ ��
(4)��֪![]() ��Һ����Ҫ����H2O��Fe3+��Cl-����������ͬѧ���������ֲ��룺
��Һ����Ҫ����H2O��Fe3+��Cl-����������ͬѧ���������ֲ��룺
����1���������ֽ�H2O2����![]() ��Һ�е�Fe3+
��Һ�е�Fe3+
����2���������ֽ�H2O2���� __________________
��ɱ�����֤���룺
�����Լ� | ���������� | ���� |
_________ | __________ | Cl-��H2O2�ֽ������� |
���𰸡��¶� ����  ��Ӧ�������ݿ��� ���������Ӳ�ͬ��ʵ��ĸ��� Cl- ˫��ˮ������ ��ʢ��H2O2��Һ���Թ��м���������HCl��Ȼ��Ѵ����ǵ�ľ�������Թ��У�ľ������ȼ
��Ӧ�������ݿ��� ���������Ӳ�ͬ��ʵ��ĸ��� Cl- ˫��ˮ������ ��ʢ��H2O2��Һ���Թ��м���������HCl��Ȼ��Ѵ����ǵ�ľ�������Թ��У�ľ������ȼ
��������
(1)���������ڳ����º��ѷֽ�õ���������ֽ��ٶ���Ũ�ȡ��¶ȡ����������ص�Ӱ�����ʵ�鷽����֤��ʱ�����Ʊ�����ȷ��ʵ������ȷ�ԣ�
(2)������ˮ�������ռ�һ���������������ʢ��ˮ����Ͳ������ʢˮ��ˮ���У����õ�����ͼ1���ӣ�
(3)�ٸ��ݷ�Ӧ��������Ŀ����������ڸ���FeCl3��![]() �������Ӳ�ͬ��������Ҳ��ͬ�������
�������Ӳ�ͬ��������Ҳ��ͬ�������
(4)����˫��ˮ��Һ����ˮ������ų�ˮ�����������ݲ���1��֪����2Ӧ���������ֽ�H2O2����Cl-��Ϊ��֤����2����ʢ��H2O2��Һ���Թ��м����������������ӵ�������˫��ˮ��Һ�к��е���������������ʵ����֤��
(1)���ݱ��и��������ݣ����������ȵ�����£���ͬŨ�ȵĹ���������Һ����������Ӧ�����������ȵ�����£���ͬŨ�ȵĹ���������Һ���ֽ⣬˵����������ķֽ��������¶��йأ����ǵõ���ͬ�����ʱ�䲻ͬ��Ũ��Խ��Ӧ���ٶ�Խ�죬˵����������ķֽ�������Ũ���йأ��Ƚ�ͬһŨ�ȵĹ���������Һ��30%ʱ�����������ȵ�ʱ����Ҫʱ����360s���д������ȵ������£���Ҫʱ����10s��˵����������ķֽ��������¶ȡ������йأ���˸��о�С������Ʒ���ʱ��������Ũ�ȡ��¶Ⱥʹ������ضԹ�������ֽ����ʵ�Ӱ�죬�ʴ�Ϊ���¶ȡ�������
(2)������ˮ�������ռ�һ�������������������ʢ��ˮ����Ͳ������ʢˮ��ˮ���У����õ�����ͼ1���ӣ�װ��ͼΪ��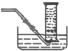 ���ʴ�Ϊ��
���ʴ�Ϊ��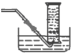 ��
��
(3)�����ڹ�������ֽ�������壬���ҷ�Ӧ���ȣ���˿��Ը��ݷ�Ӧ�в������ݵĿ������ж�Fe3+��![]() ��H2O2�ֽ�Ĵ�Ч�����ʴ�Ϊ����Ӧ�������ݿ�����
��H2O2�ֽ�Ĵ�Ч�����ʴ�Ϊ����Ӧ�������ݿ�����
��H2O2�������п�����������������ã���ΪFe2(SO4)3ʹ��������ͬ�������������������Ӳ�ͬ��ʵ��ĸ��ţ���Ϊ�������ʴ�Ϊ�����������Ӳ�ͬ��ʵ��ĸ��ţ�
(4)FeCl3��Һ����Ҫ����H2O��Fe3+��Cl-������������˫��ˮ��Һ����ˮ������ų�ˮ�����������ݲ���1��֪����2Ϊ���������ֽ�H2O2����Cl-��Ϊ��֤����2����ʢ��H2O2��Һ���Թ��м���������HCl��Ȼ��Ѵ����ǵ�ľ�������Թ��У�ľ������ȼ���ó����ۣ�Cl-��H2O2�ֽ������ã��ʴ�Ϊ��Cl-��˫��ˮ�������ʢ��H2O2��Һ���Թ��м���������HCl��Ȼ��Ѵ����ǵ�ľ�������Թ��У�ľ������ȼ��

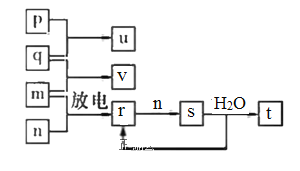
����Ŀ��Ϊ��֤�����ԣ�Cl2��Fe3+��SO2��ij��ѧ�о���ѧϰС������ͼ��ʾװ�ý���ʵ�飨�г�������A�еļ���װ�����ԣ��������Ѿ�������ϣ���
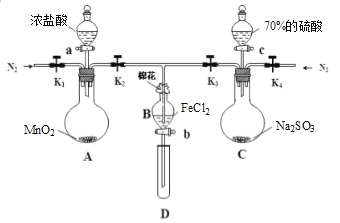
�������ɼ�K1��K4��ͨ��һ��ʱ��N2���ٽ�T�͵��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1��K3��K4��
��������a���μ�һ������Ũ���ᣬ��A������
������B����Һ���ʱ��ֹͣ���ȣ��н����ɼ�K2��
��������b��ʹԼ2mL����Һ����D�Թ��У��������е���������
�������ɼ�K3������c������70%�����ᣬһ��ʱ���н����ɼ�K3��
���������Թ�D���ظ�������������B��Һ�е�������
��1����������Ŀ����__________________________________________________________��
��2�����н������ҺΪ________________��������_____________________________________________ ��
��3��A�з�����Ӧ�Ļ�ѧ����ʽ________________________________________________��
��4�����²���������Һ��Ƶ����ӷ�Ӧ��________________________________________����________��д�Լ���ѧʽ�������������������____________________________________________ ��
��5����˵��������Fe3+��SO2�����ӷ���ʽ��_______________________________��
��6���ס��ҡ�����λͬѧ�ֱ����������ʵ�飬���ǵļ����һ���ܹ�֤��������:Cl2��Fe3+��SO2����_______��������������������������
��������B��Һ�к��е����� | ��������B��Һ�к��е����� | |
�� | ��Fe3+��Fe2+ | ��SO42�� |
�� | ����Fe3+����Fe2+ | ��SO42�� |
�� | ��Fe3+��Fe2+ | ��Fe2+ |