题目内容
用NA表示阿伏加德罗常数,下列结论能够成立的是
| A.0.1 mol·L-1的Na2CO3溶液中含有CO32-的个数是小于0.1NA |
| B.1 molFe与足量稀硝酸完全反应转移的电子数为2NA |
| C.0.2mol·L-1 CuSO4溶液加水稀释至体积增加1倍,其浓度变为0.1 mol·L-1 |
| D.4g NaOH固体溶解1L水中,所得溶液的物质的量浓度为0.1mol/L |
C
解析

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
用NA表示阿伏加德罗常数,下列叙述正确的是 ( )
| A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.0.5molC3H8分子中所含C-H共价键数为2NA |
| C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA |
D.1mol碳正离子 所含的电子数为11NA 所含的电子数为11NA |
向一定量的Fe、Fe0、Fe304的混合物中加人100mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,生成224 mL(标准状况)气体,向溶液中滴加KSCN溶液无红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量为
| A.2.8 g | B.5.6 g | C.11.2 g | D.无法计算 |
下列说法正确的是
| A.欲配制1.00L 1.00mol·L-1的NaCI溶液,可将58.5g NaC1溶于1.00L水中 |
| B.0.2mol Na2O2与足量水反应,转移电子数为0.4NA |
| C.同温同压下,质量相同的SO2气体和CO2气体的体积比等16:11 |
| D.1.0L 1.0mol ·L-l的Na2CO3水溶液中含有的氧原子数大于2NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA |
| B.常温常压下,7.0 g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C.1 mol Al3+离子含有的核外电子数为3NA |
| D.某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
NA为阿伏伽德罗常数的值.下列叙述正确的是
| A.1.0L1.0mo1·L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| B.12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| C.25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 NA |
| D.1mol的羟基与1 mol的氢氧根离子所含电子数均为9NA |
如图是某溶液在稀释过程中溶质的物质的量浓度随溶液体积的变化曲线图,根据图中数据分析可得出a值等于
| A.2 | B.3 | C.4 | D.5 |
34 g FeSO4·7H2O样品在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。下列说法中正确的是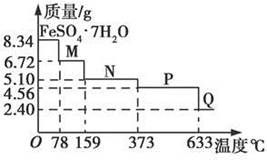
| A.温度为78℃时固体物质M的化学式为FeSO4·5H2O |
| B.温度为159℃时固体物质N的化学式为FeSO4·3H2O |
C.在隔绝空气条件下由N得到P的化学方程式为FeSO4 FeO+SO3↑ FeO+SO3↑ |
| D.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3 |