题目内容
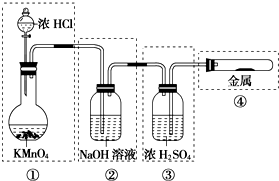 (2013?湖南模拟)已知KMnO4与浓HCl在常温下反应就能产生Cl2.若用如图所示装置来制备纯净、干燥的氯气,并试验它与金属的反应.每个虚线框表示一个单元装置,其中错误的是( )
(2013?湖南模拟)已知KMnO4与浓HCl在常温下反应就能产生Cl2.若用如图所示装置来制备纯净、干燥的氯气,并试验它与金属的反应.每个虚线框表示一个单元装置,其中错误的是( )分析:KMnO4与浓HCl在常温下反应产生Cl2,浓盐酸易挥发,生成的氯气中含有HCl和水蒸气,应通入盛有饱和食盐水的洗气瓶除去HCl,然后通入盛有浓硫酸的洗气瓶进行干燥,氯气与金属反应时,气体应通入到试管底部,并用双孔橡皮塞.
解答:解:①KMnO4与浓HCl在常温下反应产生Cl2,无需加热,盐酸易挥发,应盛装在分液漏斗中,固体放在圆底烧瓶中,故①正确;
②生成的氯气中含有HCl和水蒸气,应通入盛有饱和食盐水的洗气瓶除去HCl,氯气能与NaOH溶液反应,不能用于HCl的除杂,故②错误;
③通入洗气瓶的导管应长进短出,否则气体不能通过洗气瓶,故③错误;
④氯气与金属反应时,气体应通入到试管底部,并用双孔橡皮塞,否则会使试管内压强过大导致橡皮塞顶开,并有尾气处理装置,故④错误.
故选:D.
②生成的氯气中含有HCl和水蒸气,应通入盛有饱和食盐水的洗气瓶除去HCl,氯气能与NaOH溶液反应,不能用于HCl的除杂,故②错误;
③通入洗气瓶的导管应长进短出,否则气体不能通过洗气瓶,故③错误;
④氯气与金属反应时,气体应通入到试管底部,并用双孔橡皮塞,否则会使试管内压强过大导致橡皮塞顶开,并有尾气处理装置,故④错误.
故选:D.
点评:本题考查氯气的实验室制法,题目难度不大,注意从实验安全的角度思考.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
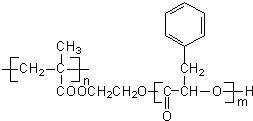 ,下列有关R的说法正确的是( )
,下列有关R的说法正确的是( )