题目内容
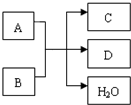 A、B、C、D是中学化学常见的物质,它们之间存在如图所示的转化关系.请按要求填空:
A、B、C、D是中学化学常见的物质,它们之间存在如图所示的转化关系.请按要求填空:(1)若A是贝壳的主要成分之一,B是厨房常见某调味品的一种成分,C常用于制作饮料,写出A与B反应的离子方程式:
(2)若A为黑色固体单质,C、D均能使澄清石灰水变浑浊,则A与B反应的化学方程式为
(3)若A为黑色粉末,C是能使石蕊试液褪色的气体,则A与B反应时还原剂与氧化剂的物质的量之比为
(4)若A为紫红色金属单质,C为无色气体,遇空气迅速变成红棕色,则产生1mol C时被氧化的A的物质的量为
(5)若A为无色晶体,易分解,分解产物之一遇C产生大量白烟,则检验A中阳离子的方法是
分析:(1)A是贝壳的主要成分之一,应为CaCO3,B是厨房常见某调味品的一种成分,应为CH3COOH,生成的C常用于制作饮料,应为CO2,则D为(CH3COO)2Ca;
(2)A为黑色固体单质,C、D均能使澄清石灰水变浑浊,应为碳和浓硫酸的反应,生成的气体为二氧化碳和二氧化硫;
(3)A为黑色粉末,C是能使石蕊试液褪色的气体,应为二氧化锰和浓盐酸的反应,C为氯气,D为氯化锰;
(4)A为紫红色金属单质,应为铜,C为无色气体,遇空气迅速变成红棕色,C应为NO,则A与B的反应为铜和稀硝酸的反应,D为硝酸铜;
(5)A为无色晶体,易分解,分解产物之一遇C产生大量白烟,可说明A为氯化铵,A与B的反应为氯化铵和氢氧化钙的反应,C为氨气,D为氯化钙.
(2)A为黑色固体单质,C、D均能使澄清石灰水变浑浊,应为碳和浓硫酸的反应,生成的气体为二氧化碳和二氧化硫;
(3)A为黑色粉末,C是能使石蕊试液褪色的气体,应为二氧化锰和浓盐酸的反应,C为氯气,D为氯化锰;
(4)A为紫红色金属单质,应为铜,C为无色气体,遇空气迅速变成红棕色,C应为NO,则A与B的反应为铜和稀硝酸的反应,D为硝酸铜;
(5)A为无色晶体,易分解,分解产物之一遇C产生大量白烟,可说明A为氯化铵,A与B的反应为氯化铵和氢氧化钙的反应,C为氨气,D为氯化钙.
解答:解:(1)A是贝壳的主要成分之一,应为CaCO3,B是厨房常见某调味品的一种成分,应为CH3COOH,生成的C常用于制作饮料,应为CO2,则D为(CH3COO)2Ca,A与B反应的离子方程式为CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,
故答案为:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑;
(2)A为黑色固体单质,C、D均能使澄清石灰水变浑浊,应为碳和浓硫酸的反应,生成的气体为二氧化碳和二氧化硫,A与B反应的化学方程式为C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,二氧化硫具有漂白性,可使品红褪色,具有还原性,可使溴水或酸性高锰酸钾溶液褪色,则可用品红、溴水或酸性高锰酸钾鉴别,
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;品红;
(3)A为黑色粉末,C是能使石蕊试液褪色的气体,应为二氧化锰和浓盐酸的反应,C为氯气,D为氯化锰,A与B反应的方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,反应中氧化剂为MnO2,还原剂为HCl,由方程式可知还原剂与氧化剂的物质的量之比为2:1,氯气可与水反应生成盐酸和次氯酸,其中次氯酸具有漂白性,可使石蕊褪色,
故答案为:2:1;氯气和水反应生成的次氯酸具有漂白性,使石蕊褪色;
(4)A为紫红色金属单质,应为铜,C为无色气体,遇空气迅速变成红棕色,C应为NO,则A与B的反应为铜和稀硝酸的反应,D为硝酸铜,
反应的方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,由方程式可知产生1molNO,则被氧化的Cu为1.5mol,
故答案为:1.5mol;
(5)A为无色晶体,易分解,分解产物之一遇C产生大量白烟,可说明A为氯化铵,A与B的反应为氯化铵和氢氧化钙的反应,C为氨气,D为氯化钙,检验A中的铵根离子,可取样于试管中,滴加NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体,或生成刺激性的气体,则证明原溶液中存在NH4+,
故答案为:取少许A置于试管中,向其中滴加NaOH溶液并加热,产生刺激性气味的气体.
故答案为:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑;
(2)A为黑色固体单质,C、D均能使澄清石灰水变浑浊,应为碳和浓硫酸的反应,生成的气体为二氧化碳和二氧化硫,A与B反应的化学方程式为C+2H2SO4(浓)
| ||
故答案为:C+2H2SO4(浓)
| ||
(3)A为黑色粉末,C是能使石蕊试液褪色的气体,应为二氧化锰和浓盐酸的反应,C为氯气,D为氯化锰,A与B反应的方程式为MnO2+4HCl(浓)
| ||
故答案为:2:1;氯气和水反应生成的次氯酸具有漂白性,使石蕊褪色;
(4)A为紫红色金属单质,应为铜,C为无色气体,遇空气迅速变成红棕色,C应为NO,则A与B的反应为铜和稀硝酸的反应,D为硝酸铜,
反应的方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,由方程式可知产生1molNO,则被氧化的Cu为1.5mol,
故答案为:1.5mol;
(5)A为无色晶体,易分解,分解产物之一遇C产生大量白烟,可说明A为氯化铵,A与B的反应为氯化铵和氢氧化钙的反应,C为氨气,D为氯化钙,检验A中的铵根离子,可取样于试管中,滴加NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体,或生成刺激性的气体,则证明原溶液中存在NH4+,
故答案为:取少许A置于试管中,向其中滴加NaOH溶液并加热,产生刺激性气味的气体.
点评:本题考查无机物的推断,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,为高考常见题型,本题考查较为综合,信息量较大,注意相关知识的学习,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
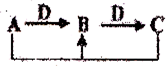 A、B、C、D是中学化学常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图,下列判断正确的是( )
A、B、C、D是中学化学常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图,下列判断正确的是( )| A、若D为H2O,A为碳,则A和C反应生成1 mol B转移的电子数为NA | ||
| B、若D为Fe,A为CI2,则B溶液蒸干后可得到纯净的B固体 | ||
| C、若D为O2,A为碱性气体,则以上转化只涉及两个氧化还原反应 | ||
D、若D为HCl,A为Na2CO3,则B溶液中c(Na+)=c(HCO3-)+2c(CO
|
 已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系.
已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系.

 已知A、B、C、D是中学化学中常见的四种不同粒子,而且均是10电子的粒子,它们之间存在如图所示的转化关系:
已知A、B、C、D是中学化学中常见的四种不同粒子,而且均是10电子的粒子,它们之间存在如图所示的转化关系:
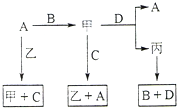 A、B、C、D 是中学化学常见的四种单质,甲、乙、丙为三种化合物,乙在常温下为无色无味的液体,各备物质间转化关系如图:(反应条件已略去),请填空:
A、B、C、D 是中学化学常见的四种单质,甲、乙、丙为三种化合物,乙在常温下为无色无味的液体,各备物质间转化关系如图:(反应条件已略去),请填空: