题目内容
(2013?泰安二模)钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,该反应的反应物与生成物有CO、Pd、H2O、HCl、PdCl2和一种未知物质X.下列说法错误的是( )
分析:CO为常见的还原剂,则钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,该反应中C元素的化合价升高,Pd元素的化合价降低,结合质量守恒定律可知发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HC1,以此来解答.
解答:解:A.由反应可知,X物质为CO2,属于氧化产物,故A正确;
B.X物质为CO2,反应中转移的电子为1 mo1时,生成
mo1物质X,故B错误;
C.反应中PdCl2作氧化剂,得电子而被还原,故C正确;
D.CO作还原剂,Pd为还原产物,则还原性为:CO>Pd,故D正确;
故选B.
B.X物质为CO2,反应中转移的电子为1 mo1时,生成
| 1 |
| 2 |
C.反应中PdCl2作氧化剂,得电子而被还原,故C正确;
D.CO作还原剂,Pd为还原产物,则还原性为:CO>Pd,故D正确;
故选B.
点评:本题考查氧化还原反应,明确CO的还原性及反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
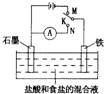 (2013?泰安二模)用如图所示装置进行实验,下列叙述不正确的是( )
(2013?泰安二模)用如图所示装置进行实验,下列叙述不正确的是( )