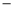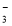题目内容
下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al+2OH-= 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- = Al(OH)3↓
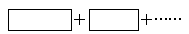
C.三氯化铁溶液中加入铁粉: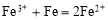
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
D
【解析】
试题分析:A.2Al+2OH-+2H2O=2AlO2-+3H2↑;错误。B.氨水是弱碱,在溶液中主要以离子的形式存在。且Al(OH)3只能被强酸、强碱溶解。因此离子方程式为:Al3++3NH3·H2O=3 NH4++Al(OH)3↓.错误;C.三氯化铁溶液中加入铁粉,没配平,电荷、电子不守恒;正确的应该是:2Fe3++Fe=3Fe2+.D,反应符合客观事实,拆写符合离子方程式的原则。正确。
考点:考查离子方程式正误判断的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案现有下列十种物质:
①H2;②铝;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩Al2(SO4)3
上述各物质按物质的分类方法填写表格的空白处(填物质编号):
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
属于该类的物质 |
|
|
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为 。
(3)⑩在水中的电离方程式为 ,
(4)少量的④通入⑥的溶液中反应的离子方程式为 。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),氧化剂与还原剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。该反应的离子方程式为 。