题目内容
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
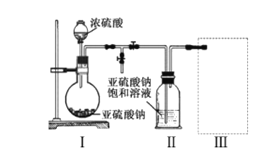
实验一 焦亚硫酸钠的制取
采用右图装置(实验前已除尽装置内的空气)制取Na2S2O5。 装置II中有Na2S2O5晶体析出,发生的反应为: Na2SO3+SO2=Na2S2O5
(1)装置1中产生气体的化学方程式为_____________________
(2)要从装置II 中获得已析出的晶体,可采取的分离方法是_____________________
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为___(填序号)。

实验二 焦亚硫酸钠的性质
已知: Na2S2O5 易被氧化,溶于水即生成NaHSO3
(4)检验Na2S2O5晶体在空气中已被氧化的实验方案是____________________。
(5)设计实验证明NaHSO3溶液中HSO3-的电离程度大于水解程度___________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。则定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)
①按上述方案实验,滴定终点的现象是______________________________。滴定时消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________kg/L。
②在上述实验过程中,若有部分HI被空气氧化,则测定结果____________(填“偏高”“偏低”或“不变”)。
【答案】 Na2SO3+H2SO4=Na2SO4+SO2↑+H2O(或Na2SO3+2H2SO4=2NaHSO4+SO2↑+H2O) 过滤 d 取少量Na2S2O5晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成 测定NaHSO3溶液pH值,若pH<7,则HSO3-的电离程度大于水解程度 滴入最后一滴溶液,溶液颜色由无色变为蓝色,且30s内不褪色 1.6×10-4 偏低
【解析】本题主要考查对于有关焦亚硫酸钠探究实验的评价。
(1)装置1中发生“强酸制弱酸”的反应,产生二氧化硫气体,反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O(或Na2SO3+2H2SO4=2NaHSO4+SO2↑+H2O)
(2)要从装置II中获得已析出的晶体,可采取的分离方法是过滤。
(3)a.二氧化硫不能与氨水充分作用,稀氨水吸收二氧化硫的能力有限,封闭装置不安全;b.食盐水吸收二氧化硫的能力有限,溶解过程存在可逆反应而使溶解不完全,二氧化硫与食盐水的作用受到限制;c.二氧化硫不溶于浓硫酸;d.二氧化硫可充分被氢氧化钠溶液吸收,该装置还可以防止倒吸。故选d。
(4)Na2S2O5可被空气中氧气氧化为Na2SO4,Na2S2O5遇盐酸会转化为SO2,检验Na2S2O5晶体在空气中已被氧化就是检验晶体中含有Na2SO4,应在除去可能存在的Na2S2O5的前提下,将Na2SO4转化为硫酸钡沉淀。实验方案是取少量Na2S2O5晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成。
(5)证明NaHSO3溶液中HSO3-的电离程度大于水解程度就是证明NaHSO3溶液呈酸性,实验方法:测定NaHSO3溶液pH值,若pH<7,则HSO3-的电离程度大于水解程度。
(6)①按上述方案实验,当上述滴定反应完成时,过量的标准I2溶液遇淀粉变蓝色,所以滴定终点的现象是滴入最后一滴溶液,溶液颜色由无色变为蓝色,且30s内不褪色。滴定时消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为0.01000mol/L×25.00mL×64g/mol/100mL=1.6×10-4kg/L。
②在上述实验过程中,若有部分HI被空气氧化,使得消耗标准I2溶液体积减少,则测定结果偏低。