��Ŀ����
����Ŀ����չ��ѧ��ѧʵ���о��������塣ͨ���о������Է���һЩʵ��װ�õIJ��㣬�Ӷ����ڴ˻����ϸĽ�ʵ�֡�
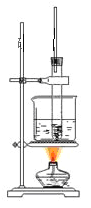
��1��ͼ��Ϊij�汾�̲���ͭ��Ũ���ᷴӦ��ʵ��װ�á�
��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��________________________��
��װ��������������Һ��������___________________________��
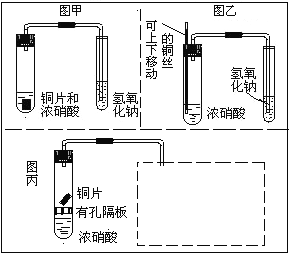
��2��С���Ը�ʵ�������ͼ�ҵĸĽ���װ���Һͼ���ȣ�ʵ������о��е��ŵ���___________��
��3����ͼ����ʾװ�ý���ʵ��ʱ��С���������³鶯ͭ˿ʱ�������Թ�����������������ľ���ݳ�����������ͼ���ĸĽ���
��������ͼװ���ռ�һ�Թ�NO2�����ڷ����ڻ�����Ӧ��װ��ͼ________��
��������ͼװ�ý���ʵ�飬ʵ����Ҳ�����ҵ��ŵ㡣Ҫʵ����һ�ŵ㣬ʵ�������Ӧ���еIJ�����____________________________________________________��
���𰸡� 3Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O ���շ�Ӧ���ɵĶ������������壬��ֹ������Ⱦ ����ʱ���Ʒ�Ӧ�ķ�����ֹͣ 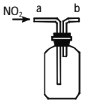 ������Թ���б��ʹŨ������ͭƬ�Ӵ�����Ӧ��������Ҫʹ��Ӧֹͣ�����Թ�ֱ������
������Թ���б��ʹŨ������ͭƬ�Ӵ�����Ӧ��������Ҫʹ��Ӧֹͣ�����Թ�ֱ������
����������1����ͭ��Ũ���ᷴӦ��������ͭ������������ˮ���ݴ�д������ʽ��
�ڶ���������һ�ִ�����Ⱦ���Ҫβ���������ݴ˷�����
��2��װ�������п������ƶ���ͭ˿��������ʱ���Ʒ�Ӧ������ֹͣ��
��3����NO2���ܶȱȿ�����������ˮ��Ӧ��Ӧ�������ſ������ռ���
��ͭƬ��Ũ����Ӵ�ʱ�����ɷ�����Ӧ�����Խ�����Թ���б���ݴ˷�����
��1����ͭ��Ũ���ᷴӦ��������ͭ������������ˮ����ѧ����ʽ��3Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O����ȷ�𰸣�3Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O��
������������Һ������������巴Ӧ�������������������ƺ�ˮ������װ��������������Һ�����������շ�Ӧ���ɵĶ������������壬��ֹ������Ⱦ����ȷ�������շ�Ӧ���ɵĶ������������壬��ֹ������Ⱦ��
��2��С���Ը�ʵ�������ͼ�ҵĸĽ���װ���Һͼ���ȣ�ʵ������о��е��ŵ��ǣ�װ�������п������ƶ���ͭ˿������ʱ���Ʒ�Ӧ�ķ�����ֹͣ����ȷ�𰸣�����ʱ���Ʒ�Ӧ�ķ�����ֹͣ��
��3����NO2���ܶȱȿ�������ˮ������Ӧ��ֻ���������ſ������ռ���������Ӧ�������̳������ռ�װ��ͼΪ ����ȷ����
����ȷ���� ��
��
��ͼ��װ����Ҫ��ʱ���Ʒ�Ӧ�ķ�����ֹͣ����ͨ��������Թ���б��ʹŨ������ͭƬ�Ӵ�����Ӧ��������Ҫʹ��Ӧֹͣ�����Թ�ֱ�����ɣ���ȷ�𰸣�������Թ���б��ʹŨ������ͭƬ�Ӵ�����Ӧ��������Ҫʹ��Ӧֹͣ�����Թ�ֱ�����ɡ�

����Ŀ��ij��ѧС��̽������������N03 -��S042-��Fe3+��������������ǿ�����������ʵ�飨�г���������ȥ��װ�õ��������Ѽ���)�� (���������Է�Ӧ��Ӱ�죩
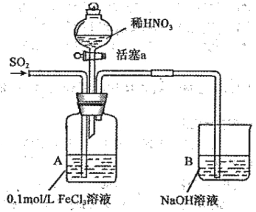
ʵ���¼����:
ʵ�� ��� | ʵ����� | '...!ʵ������ |
I | ��Aװ����ͨ��һ��ʱ���SO2���塣. | A��gɫ��Һ���ձ�Ϊdz��ɫ�� |
II | ȡ������Aװ���е����ƣ��ȼ��� KSCN��Һ���ټ���BaCl2��Һ�� | ����KSCN��Һ����Һ����ɫ;�ټ���BaCl2��Һ������ɫ������ |
III | ����a��������ϡHNO3����װ��A �У��رջ���a�� | A��dz��ɫ��Һ���ձ�Ϊ��ɫ�� |
IV | ȡ������Aװ���е���Һ������KSCN ��Һ�� | ��Һ��Ϊ��ɫ�� |
��ش��������⣺
��1��д��Aװ����ͨ�˶����������巢����Ӧ�����ӷ���ʽ ��
��2��ʵ��II�з�����Ӧ�����ӷ���ʽ�� ��
��3��ʵ��III�У�dz��ɫ��Һ��Ϊ��ɫ��ԭ���� ��(��������������
��4��ʵ��IV����A��ͨ���˿�����Һ���Ϸ��������� ��
��5���ۺ�����ʵ��Ì�Ľ�����:�����������£�������ǿ��˳��Ϊ ��