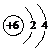题目内容
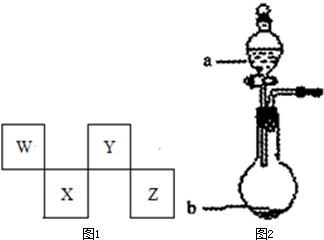
W、X、Y、Z四种短周期元素在元素周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数l:1和1:2的化合物.
请回答下列问题.
(1)W元素形成的同素异形体的晶体类型可能是(填序号) .
①原子晶体 ②离子晶体③分子晶体 ④金属晶体
(2)H2Y2的电子式为 ,Na2Y2中的化学键种类为: .
(3)在图2中,b的pH约为7,且含有Fe2+和淀粉KI的水溶液,a为H2Y2的水溶液,旋开分液漏斗旋钮,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成.当消耗2molI-时,共转移3mol电子,该反应的离子方程式是 .
(4)已知:298K时,金属钠与Y2气体反应,若生成1molNa2Y固体时,放出热量414kJ;若生成1mol Na2Y2固体时,放出热量511kJ.则由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为 .
(5)X的原子结构示意图为 .Z在周期表中的位置 .
(6)有人设想利用原电池原理以气体Z2和氢气制备一种重要的化工原料,同时获取电能.假设这种想法可行,用石墨作电极材料,用稀盐酸作电解质溶液,则通入Z2的电极为原电池的 极,其电极反应式为 .

请回答下列问题.
(1)W元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体③分子晶体 ④金属晶体
(2)H2Y2的电子式为
(3)在图2中,b的pH约为7,且含有Fe2+和淀粉KI的水溶液,a为H2Y2的水溶液,旋开分液漏斗旋钮,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成.当消耗2molI-时,共转移3mol电子,该反应的离子方程式是
(4)已知:298K时,金属钠与Y2气体反应,若生成1molNa2Y固体时,放出热量414kJ;若生成1mol Na2Y2固体时,放出热量511kJ.则由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为
(5)X的原子结构示意图为
(6)有人设想利用原电池原理以气体Z2和氢气制备一种重要的化工原料,同时获取电能.假设这种想法可行,用石墨作电极材料,用稀盐酸作电解质溶液,则通入Z2的电极为原电池的
分析:W、X、Y、Z四种短周期元素,由元素在元素周期表中的位置,可知W、Y处于第二周期,X、Z处于第三周期,其中Y与钠元素和氢元素均可形成原子个数l:1和1:2的化合物,则Y为O元素,可推知W为C元素、X为P、Z为Cl,
(1)碳单质同素异形体有金刚石、石墨、C60等,金刚石为原子晶体、C60为分子晶体,石墨为混合晶体;
(2)H2O2分子中O原子之间形成1对共用电子对、H原子与O原子之间形成1对共用电子对;Na2O2属于离子化合物,过氧根离子中O原子之间形成非极性键;
(3)在图2中,将H2O2的水溶液滴入含有Fe2+和淀粉KI的水溶液,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成,说明反应生成氢氧化铁与碘单质.当消耗2molI-时,共转移3mol电子,则参加反应的Fe2+物质的量为
=1mol,参加反应H2O2的物质的量=
=1.5mol,故Fe2+、H2O2、I-的化学计量数之比=2:3:4,据此书写;
(4)根据题意书写Na与氧气反应生成氧化钠、过氧化钠的热化学方程式,再根据盖斯定律书写;
(5)P原子核外电子数为15,有3个电子层,最外层电子数为5;Z为Cl元素,处于第三周期ⅦA族;
(6)氯气获得电子生成Cl-,发生还原反应,应在原电池正极通入.
(1)碳单质同素异形体有金刚石、石墨、C60等,金刚石为原子晶体、C60为分子晶体,石墨为混合晶体;
(2)H2O2分子中O原子之间形成1对共用电子对、H原子与O原子之间形成1对共用电子对;Na2O2属于离子化合物,过氧根离子中O原子之间形成非极性键;
(3)在图2中,将H2O2的水溶液滴入含有Fe2+和淀粉KI的水溶液,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成,说明反应生成氢氧化铁与碘单质.当消耗2molI-时,共转移3mol电子,则参加反应的Fe2+物质的量为
| 3mol-2mol |
| 3-2 |
| 3mol |
| 2×[(-1)-(-2)] |
(4)根据题意书写Na与氧气反应生成氧化钠、过氧化钠的热化学方程式,再根据盖斯定律书写;
(5)P原子核外电子数为15,有3个电子层,最外层电子数为5;Z为Cl元素,处于第三周期ⅦA族;
(6)氯气获得电子生成Cl-,发生还原反应,应在原电池正极通入.
解答:解:W、X、Y、Z四种短周期元素,由元素在元素周期表中的位置,可知W、Y处于第二周期,X、Z处于第三周期,其中Y与钠元素和氢元素均可形成原子个数l:1和1:2的化合物,则Y为O元素,可推知W为C元素、X为P、Z为Cl,
(1)碳单质同素异形体有金刚石、石墨、C60等,金刚石为原子晶体、C60为分子晶体,石墨为混合晶体,
故答案为:①③;
(2)H2O2分子中O原子之间形成1对共用电子对、H原子与O原子之间形成1对共用电子对,其电子式为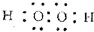 ;Na2O2属于离子化合物,过氧根离子中O原子之间形成非极性键,含有离子键、非极性键,
;Na2O2属于离子化合物,过氧根离子中O原子之间形成非极性键,含有离子键、非极性键,
故答案为: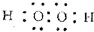 ;离子键、非极性;
;离子键、非极性;
(3)在图2中,将H2O2的水溶液滴入含有Fe2+和淀粉KI的水溶液,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成,说明反应生成氢氧化铁与碘单质.当消耗2molI-时,共转移3mol电子,则参加反应的Fe2+物质的量为
=1mol,参加反应H2O2的物质的量=
=1.5mol,故Fe2+、H2O2、I-的化学计量数之比=2:3:4,该反应离子方程式为:2Fe2++3H2O2+4I-=2Fe(OH)3+2I2,
故答案为:2Fe2++3H2O2+4I-=2Fe(OH)3+2I2;
(4)根据题意可知:①2Na(s)+
O2(g)=Na2O(s)△H=-414kJ/mol
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ/mol
根据盖斯定律,②-①得Na2O(s)+
O2(g)=Na2O2(s)△H=-97kJ/mol,
故答案为:Na2O(s)+
O2(g)=Na2O2(s)△H=-97kJ/mol;
(5)P原子核外电子数为15,有3个电子层,最外层电子数为5,原子结构示意图为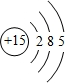 ;Z为Cl元素,处于第三周期ⅦA族,
;Z为Cl元素,处于第三周期ⅦA族,
故答案为: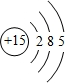 ;第三周期ⅦA族;
;第三周期ⅦA族;
(6)氯气获得电子生成Cl-,发生还原反应,应在原电池正极通入,电极反应式为:Cl2+2e-=2Cl-,
故答案为:正;Cl2+2e-=2Cl-.
(1)碳单质同素异形体有金刚石、石墨、C60等,金刚石为原子晶体、C60为分子晶体,石墨为混合晶体,
故答案为:①③;
(2)H2O2分子中O原子之间形成1对共用电子对、H原子与O原子之间形成1对共用电子对,其电子式为
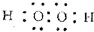 ;Na2O2属于离子化合物,过氧根离子中O原子之间形成非极性键,含有离子键、非极性键,
;Na2O2属于离子化合物,过氧根离子中O原子之间形成非极性键,含有离子键、非极性键,故答案为:
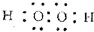 ;离子键、非极性;
;离子键、非极性;(3)在图2中,将H2O2的水溶液滴入含有Fe2+和淀粉KI的水溶液,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成,说明反应生成氢氧化铁与碘单质.当消耗2molI-时,共转移3mol电子,则参加反应的Fe2+物质的量为
| 3mol-2mol |
| 3-2 |
| 3mol |
| 2×[(-1)-(-2)] |
故答案为:2Fe2++3H2O2+4I-=2Fe(OH)3+2I2;
(4)根据题意可知:①2Na(s)+
| 1 |
| 2 |
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ/mol
根据盖斯定律,②-①得Na2O(s)+
| 1 |
| 2 |
故答案为:Na2O(s)+
| 1 |
| 2 |
(5)P原子核外电子数为15,有3个电子层,最外层电子数为5,原子结构示意图为
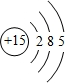 ;Z为Cl元素,处于第三周期ⅦA族,
;Z为Cl元素,处于第三周期ⅦA族,故答案为:
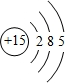 ;第三周期ⅦA族;
;第三周期ⅦA族;(6)氯气获得电子生成Cl-,发生还原反应,应在原电池正极通入,电极反应式为:Cl2+2e-=2Cl-,
故答案为:正;Cl2+2e-=2Cl-.
点评:本题以元素推断为载体,考查常用化学用语、化学键、氧化还原反应、热化学方程式、原电池等,难度中等,(3)中离子方程式书写,为易错点,需要根据电子转移计算确定化学计量数.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,下列判断不正确的是( )
| W | X | |
| Y | Z |
| A、原子半径大小:W>X |
| B、元素最高正价:W>Z |
| C、简单阴离子的还原性:Y>Z |
| D、气态氢化物的稳定性:X>Y |
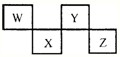 W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.
W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.