题目内容
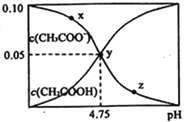
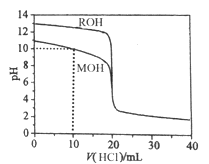
【题目】常温下,用浓度为0.1000mol/L的盐酸分别逐滴加入到20.00mL 0.1000mol/L的两种一元碱MOH、ROH溶液中,PH随盐酸溶液体积的变化如图所示。下列说法正确的是
A. PH=10时,c(M+)>c(MOH)>c(Cl-)>c(OH-)>c(H+)
B. 将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时:c(R+)>c(M+)>c(H+)>c(OH-)
C. 10mL<V(HCl)<20mL时,c(M+)+c(NOH)<c(Cl-)
D. V(HCl)>20mL时,不可能存在:c(Cl-)>c(M+)=c(H+)>c(OH-)
【答案】B
【解析】PH=10时,加入盐酸10 mL,溶质为等物质的量的MCl和MOH ,溶液呈碱性,说明MOH电离大于MCl水解,c(M+)>c(Cl-)>c(MOH)>c(OH-)>c(H+),故A错误;根据图像0.1000mol/L一元碱MOH、ROH的PH分别是13和11,则溶液MOH是强碱、ROH是弱碱,用盐酸滴定至MOH恰好反应时,恰好生成等物质的量的MCl和RCl,MCl水解呈碱性,所以c(R+)>c(M+)>c(H+)>c(OH-),故B正确;10mL<V(HCl)<20mL时,MOH 的物质的量小于盐酸的物质的量,所以c(M+)+c(MOH)>c(Cl-),故C错误;当盐酸剩余大约一半时,根据电荷守恒,c(Cl-)+ c(OH-)=c(M+)+c(H+),存在:c(Cl-)>c(M+)=c(H+)>c(OH-),故D错误。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案【题目】向1 L含0.01 mol NaAlO2和0.02 mol NaOH的溶液中缓慢通入CO2,随n(CO2)增大,先后发生三个不同的反应,当0.01 mol<n(CO2) ![]() 0.015时发生的反应是:2 NaAlO2+ CO2+3H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
0.015时发生的反应是:2 NaAlO2+ CO2+3H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |