题目内容
黄铜矿(CuFeS2)常用于提炼金属铜。黄铜矿焙烧过程中所发生的反应比较复杂,其中主要反应之一的化学方程式为2CuFeS2+O2=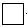 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是
 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是| A.方框中的物质应为Cu2S |
| B.该反应的部分产物可用于硫酸工业 |
| C.反应中SO2既是氧化产物又是还原产物 |
| D.反应中若有1molSO2生成,则一定有4mol电子发生转移 |
D
试题分析:A根据质量守恒定律可知方框中的物质为硫化亚铜,正确。B因为产生了二氧化硫,所以可用于工业制取硫酸,正确。C硫化合价从CuFeS2-2→SO2的+4,化合价升高,失去电子,作还原剂,SO2是氧化产物;氧元素的化合价从O2的0,→SO2的-2,化合价降低,得到电子,作氧化剂,SO2是还原产物。正确。D在该反应中,若有1molSO2生成,则有6mol电子发生转移.错误。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
 Cl- OH- CO
Cl- OH- CO

 Cu2++
Cu2++