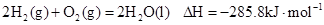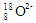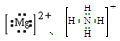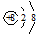题目内容
已知:Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,常温下能氧化浓HCl生成Cl2;PbO2不稳定,随温度升高按下列顺序逐步分解:PbO2→Pb2O3→Pb3O4→PbO。
现将a mol PbO2加热分解,收集产生的O2;加热反应后所得固体中,Pb2+占Pb元素的物质的量分数为x;向加热后所得固体中加入足量的浓盐酸,收集产生的Cl2。两步反应中收集的O2和Cl2的物质的量之和为y mol。
(1)若Fe3O4可表示为FeO·Fe2O3,则Pb2O3可表示为
(2)试写出Pb2O3与浓盐酸反应的化学方程式
(3)通过计算确定y与a、x的函数关系式____________________________。
现将a mol PbO2加热分解,收集产生的O2;加热反应后所得固体中,Pb2+占Pb元素的物质的量分数为x;向加热后所得固体中加入足量的浓盐酸,收集产生的Cl2。两步反应中收集的O2和Cl2的物质的量之和为y mol。
(1)若Fe3O4可表示为FeO·Fe2O3,则Pb2O3可表示为
(2)试写出Pb2O3与浓盐酸反应的化学方程式
(3)通过计算确定y与a、x的函数关系式____________________________。
(1)PbO .Pb2O3
(2)Pb2O3+6HCl→2 Pb Cl2+Cl2+3H2O
(3)y=a(1-0.5x)
(2)Pb2O3+6HCl→2 Pb Cl2+Cl2+3H2O
(3)y=a(1-0.5x)
略

练习册系列答案
相关题目
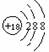



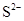 的结构示意图:
的结构示意图:

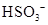 离子的电离方程式:
离子的电离方程式: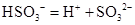
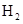 在25℃ 101kpa下燃烧,生成液态的水放出285.8
在25℃ 101kpa下燃烧,生成液态的水放出285.8 U的热量,则该反应的热化学方程式为:
U的热量,则该反应的热化学方程式为: