题目内容
【题目】将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示。下列说法不正确的是
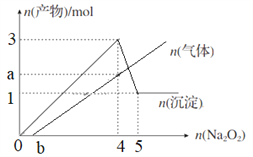
A. a=1.75
B. b=0.5
C. 原溶液中Al3+与Fe2+的物质的量之比为1:2
D. 最后得到的沉淀为Fe(OH)3
【答案】C
【解析】Na2O2加入到含Al3+、Fe2+的混合液中,Na2O2与水反应生成NaOH和O2,O2将Fe2+氧化成Fe3+,Al3+、Fe3+与NaOH形成沉淀Al(OH)3和Fe(OH)3沉淀,Al3+、Fe3+完全沉淀后,Al(OH)3溶于NaOH。A项,由图中纵坐标知n[Al(OH)3]=2mol,n[Fe(OH)3]=1mol,根据Fe守恒原溶液中n(Fe2+)=1mol,根据得失电子守恒,将Fe2+氧化的O2物质的量为n(O2)=n(Fe2+)/4=0.25mol,根据反应2Na2O2+2H2O=4NaOH+O2↑,当加入4molNa2O2时反应生成8molNaOH和2molO2,则a点O2物质的量为2mol-0.25mol=1.75mol,正确;B项,Fe2+被氧化消耗0.25molO2,根据反应2Na2O2+2H2O=4NaOH+O2↑,生成0.25molO2消耗0.5molNa2O2,即b=0.5,正确;C项,根据Al守恒,原溶液中n(Al3+)= n[Al(OH)3]=2mol,原溶液中Al3+与Fe2+物质的量之比为2:1,错误;D项,最后Al(OH)3全部溶解,最后的沉淀为Fe(OH)3,正确;答案选C。

【题目】(1)完成下列表格
主要物质 | 杂质 | 除杂试剂 | 操作名称 |
CO2气体 | HCl气体 | _______ | _______ |
FeCl2溶液 | CuCl2 | _______ | _______ |
水 | 花生油 | _______ |
(2)用双线桥法表述(只标注电子转移情况):MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O___________。
MnCl2+Cl2↑+2H2O___________。
用单线桥法表述电子转移情况:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O___________。
(3)用所给量的符号和必要的数据,按要求列出相关计算式:
①摩尔质量为M,气体摩尔体积为Vm,则气体体积V与气体质量m的关系___________。
②物质的量浓度为c,溶质摩尔质量为M,则溶液体积V与所含溶质质量m的关系____。
③溶质摩尔质量为M,溶液密度为dg/ml,则物质的量浓度c与溶质质量分数a%的关系c=__。
④摩尔质量为M,气体摩尔体积为Vm,则气体的密度=______________。
⑤某条件下气体摩尔体积为Vm,将V升某气体(摩尔质量为M)溶于1升水,得到密度为dg/mL的溶液,则该溶液的物质的量浓度c=_______。