题目内容
充分完全燃烧一定量的乙烯与常温下呈气态的某烃混合气体后,测得其生成物中气体的质量是反应前混合烃质量的2.86倍,试通过计算确定该气态烃的分子式及它在该混合烃气体中所占的物质的量分数(气体质量为常温下所得)。
CH4 81.82%
解析:(解法一)C2H4生成CO2与原C2H4质量比:![]() =3.12>2.86
=3.12>2.86
另一烃CxHy生成的CO2与原CxHy质量比:![]()
由平均值原理可知:![]() <2.86
<2.86
约![]() >3.38,符合条件的只有CH4。
>3.38,符合条件的只有CH4。
设CH4为a mol,则为![]() =2.86
=2.86
得a=0.818 2,CH4所占的物质的量百分含量为:![]() ×100%=81.82%
×100%=81.82%
(解法二)设混合烃100 g,其中CxHy为a g,则有:![]() ×44x+
×44x+![]() ×88=286
×88=286
整理得:a=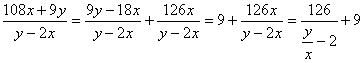
因为a<100,可得:![]() >3.38
>3.38
所以满足此条件的烃只有CH4。

练习册系列答案
相关题目