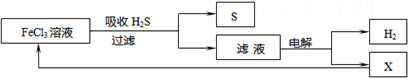
��Ŀ����
��2013?�ֶ�������ģ��ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ�飨ͼ��a��b��c��ʾֹˮ�У���
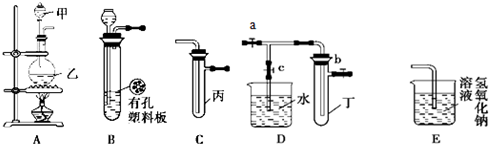
�밴Ҫ����գ�?
��1������Bװ�ÿ���ȡ��������
��2��A��C��E�������װ�ÿ�������ȡCl2��������ص�����ʵ�飮
���ڱ��м�������ˮ�������Ƶ���ˮ����������ˮ�ֳ����ݣ����Т�����ʵ�飬ʵ�����������������£�?
��������ʵ���Ľ����Ƿ������������������˵�����ɣ�
��3������������A��Cװ�����һ����ʵ�飬��֤Cl2��Br2��������ǿ�����ֱ�ָ���ס��ҡ�����ʢװ���Լ���ʵ�������ۣ�
��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ
��5������Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ��
��6���Թܶ��е�NO2��һ������O2��Ϻ�ˮ�У��Թ�9/10����ˮ����ԭ�Թܶ��еĻ�������ƽ������������Ϊ

�밴Ҫ����գ�?
��1������Bװ�ÿ���ȡ��������
H2��CO2��H2S��
H2��CO2��H2S��
����2�֣�����2��A��C��E�������װ�ÿ�������ȡCl2��������ص�����ʵ�飮
���ڱ��м�������ˮ�������Ƶ���ˮ����������ˮ�ֳ����ݣ����Т�����ʵ�飬ʵ�����������������£�?
| ʵ����� | ʵ����� | ���� | ���� |
| �� | ����ˮ����Ʒ����Һ | ��Һ��ɫ | ������ˮ��Ӧ�IJ�����Ư���� |
| �� | ��ˮ�м��� NaHCO3��ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ�IJ�����н�ǿ������ |
��������û������֤�������������Ư���ԣ�����������ȡ�������к���HCl���壬HCl����ˮ������̼�����Ʒ�ĩ��Ӧ��������
��������û������֤�������������Ư���ԣ�����������ȡ�������к���HCl���壬HCl����ˮ������̼�����Ʒ�ĩ��Ӧ��������
����3������������A��Cװ�����һ����ʵ�飬��֤Cl2��Br2��������ǿ�����ֱ�ָ���ס��ҡ�����ʢװ���Լ���ʵ�������ۣ�
�ڼס��ҡ����зֱ�װ��Ũ���ᡢ�������̡��廯����Һ����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ����֤��������������ǿ����
�ڼס��ҡ����зֱ�װ��Ũ���ᡢ�������̡��廯����Һ����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ����֤��������������ǿ����
��B��D��Eװ����������B��ʢװ����Ũ�����ͭƬ�������п����ϰ��ϣ������Ƶ�NO2�������й�ʵ�飮��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ
Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O
Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O
����5������Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ��
a��b
a��b
���ٴ�ֹˮ��c
c
��ʹ�ձ��е�ˮ�����Թܶ��IJ�����˫�ֽ��գ����ȣ��Թܶ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ�
˫�ֽ��գ����ȣ��Թܶ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ�
����6���Թܶ��е�NO2��һ������O2��Ϻ�ˮ�У��Թ�9/10����ˮ����ԭ�Թܶ��еĻ�������ƽ������������Ϊ
42.08��44.04
42.08��44.04
����������λС������������1��Bװ��Ϊ��״������ˮ�Ĺ����Һ�巴Ӧ��������ȡ�����װ�ã�
��2��ʵ�����Ƶõ�����������������ˮ�������Ȼ������壬�����ܺ�̼�����Ʒ�Ӧ����������̼���壻
��3����֤Cl-��Br-�Ļ�ԭ��ǿ���ɸ��ݷ�ӦCl2+2Br-=2Cl-+Br2���ʵ�飻
��4��Ũ�������ǿ�����ԣ���ͭ��Ӧ���ɶ����������壻
��5��NO2��ˮ��Ӧ������ɫ����NO��
��6�����жϹ���������ijɷ֣���Ϊ������Ȼ����� 4NO2+O2+2H2O=4HNO3���㣬����μӴ˷�Ӧ��NO2��O2�������ӵõ�ԭ������������ΪNO���ȸ���3NO2+H2O=2HNO3+2NO���������NO2��Ȼ�����4NO2+O2+2H2O=4HNO3����μӴ˷�Ӧ��NO2��O2�������ӵõ�ԭ����NO2�����ո���M=
��ƽ��Ħ��������ƽ����������Ħ����������ֵ����ȣ�
��2��ʵ�����Ƶõ�����������������ˮ�������Ȼ������壬�����ܺ�̼�����Ʒ�Ӧ����������̼���壻
��3����֤Cl-��Br-�Ļ�ԭ��ǿ���ɸ��ݷ�ӦCl2+2Br-=2Cl-+Br2���ʵ�飻
��4��Ũ�������ǿ�����ԣ���ͭ��Ӧ���ɶ����������壻
��5��NO2��ˮ��Ӧ������ɫ����NO��
��6�����жϹ���������ijɷ֣���Ϊ������Ȼ����� 4NO2+O2+2H2O=4HNO3���㣬����μӴ˷�Ӧ��NO2��O2�������ӵõ�ԭ������������ΪNO���ȸ���3NO2+H2O=2HNO3+2NO���������NO2��Ȼ�����4NO2+O2+2H2O=4HNO3����μӴ˷�Ӧ��NO2��O2�������ӵõ�ԭ����NO2�����ո���M=
| m�� |
| n�� |
����⣺��1��Bװ��Ϊ��״������ˮ�Ĺ����Һ�巴Ӧ��ȡ�����װ�ã������ü��ȣ���ѧ��ѧ�г������У�H2��CO2��H2S �ȣ��ʴ�Ϊ��H2��CO2��H2S �ȣ�
��2��ʵ�����Ƶõ�����������������ˮ�������Ȼ������壬Ҫ���и�����������߱�Ư���Ե���֤���飬�ٽ���ʵ�����ܵõ����ۣ��Ȼ�����������ˮ�γ����ᣬ����Ҳ�ܺ�̼�����Ʒ�Ӧ����������̼���壬��һ����������ˮ��Ӧ�IJ�������ԣ��ʴ�Ϊ����������û������֤�������������Ư���ԣ��������� ��ȡ�������к���HCl���壬HCl����ˮ������̼�����Ʒ�ĩ��Ӧ�������ݣ�
��3����֤Cl-��Br-�Ļ�ԭ��ǿ���ɸ��ݷ�ӦCl2+2Br-=2Cl-+Br2���ʵ�飬��Aװ�����Ʊ����������ɵ�����ͨ�뵽װ���廯����Һ��C�У�����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ����֤��������������ǿ���壬
�ʴ�Ϊ���ڼס��ҡ����зֱ�װ��Ũ���ᡢ�������̡��廯����Һ����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ����֤��������������ǿ���壻
��4��Ũ�������ǿ�����ԣ���ͭ��Ӧ���ɶ����������壬��Ӧ�Ļ�ѧ����ʽΪCu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O��
�ʴ�Ϊ��Cu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O��
��5��Ũ������ͭ��Ӧ���ɵĶ��������ռ����Թܶ��У�װ����֤NO2��ˮ�ķ�Ӧ��Ҫ�ȹر�a��b��Ȼ�����ȷ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ��У�
�ʴ�Ϊ��a��b��c��˫�ֽ��գ����ȣ��Թܶ���ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ��У�
��6��NO2��O2���������Թܵ�����ˮ�У�������Ӧ��4NO2+O2+2H2O=4HNO3 ���ʣ���������Ϊ������Ҳ������NO���壬��NO2��O2�����������ʵ���Ϊ10mol��
��ʣ������Ϊ��������μ�4NO2+O2+2H2O=4HNO3 ��Ӧ���ĵ�����Ϊx���������ĵ�NO2Ϊ4x������5x=9mol��x=1.8mol��������Ϊ2.8mol��V��NO2��=7.2mol��
��������������Ϊ7.2molNO2��2.8molO2������֮��Ϊ7.2mol��46g/mol+2.8mol��32g/mol=420.8g��ƽ��Ħ������
=42.08g/mol��ƽ��������42.08��
��ʣ������ΪNO���壬�Թ�9/10����ˮ����ʣ��1molNO������3NO2+H2O=2HNO3+NO��˵��������NO2Ϊ3mol����Ӧ4NO2+O2+2H2O=4HNO3���ĵ����������Ϊ7mol���跴Ӧ���ĵ�����Ϊy���������ĵ�NO2Ϊ4y����5y=7mol��y=1.4mol������ʱ����Ϊ1.4mol��V��NO2��=8.6mol��
��������������Ϊ8.6molNO2��1.4molO2������֮��Ϊ8.6mol��46g/mol+1.4mol��32g/mol=440.4g��ƽ��Ħ������
=44.04g/mol��ƽ��������44.04��
�ʴ�Ϊ��42.08��44.04��
��2��ʵ�����Ƶõ�����������������ˮ�������Ȼ������壬Ҫ���и�����������߱�Ư���Ե���֤���飬�ٽ���ʵ�����ܵõ����ۣ��Ȼ�����������ˮ�γ����ᣬ����Ҳ�ܺ�̼�����Ʒ�Ӧ����������̼���壬��һ����������ˮ��Ӧ�IJ�������ԣ��ʴ�Ϊ����������û������֤�������������Ư���ԣ��������� ��ȡ�������к���HCl���壬HCl����ˮ������̼�����Ʒ�ĩ��Ӧ�������ݣ�
��3����֤Cl-��Br-�Ļ�ԭ��ǿ���ɸ��ݷ�ӦCl2+2Br-=2Cl-+Br2���ʵ�飬��Aװ�����Ʊ����������ɵ�����ͨ�뵽װ���廯����Һ��C�У�����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ����֤��������������ǿ���壬
�ʴ�Ϊ���ڼס��ҡ����зֱ�װ��Ũ���ᡢ�������̡��廯����Һ����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ����֤��������������ǿ���壻
��4��Ũ�������ǿ�����ԣ���ͭ��Ӧ���ɶ����������壬��Ӧ�Ļ�ѧ����ʽΪCu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O��
�ʴ�Ϊ��Cu+4HNO3��Ũ���TCu��NO3��2+2NO2��+2H2O��
��5��Ũ������ͭ��Ӧ���ɵĶ��������ռ����Թܶ��У�װ����֤NO2��ˮ�ķ�Ӧ��Ҫ�ȹر�a��b��Ȼ�����ȷ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ��У�
�ʴ�Ϊ��a��b��c��˫�ֽ��գ����ȣ��Թܶ���ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ��У�
��6��NO2��O2���������Թܵ�����ˮ�У�������Ӧ��4NO2+O2+2H2O=4HNO3 ���ʣ���������Ϊ������Ҳ������NO���壬��NO2��O2�����������ʵ���Ϊ10mol��
��ʣ������Ϊ��������μ�4NO2+O2+2H2O=4HNO3 ��Ӧ���ĵ�����Ϊx���������ĵ�NO2Ϊ4x������5x=9mol��x=1.8mol��������Ϊ2.8mol��V��NO2��=7.2mol��
��������������Ϊ7.2molNO2��2.8molO2������֮��Ϊ7.2mol��46g/mol+2.8mol��32g/mol=420.8g��ƽ��Ħ������
| 420.8g |
| 10mol |
��ʣ������ΪNO���壬�Թ�9/10����ˮ����ʣ��1molNO������3NO2+H2O=2HNO3+NO��˵��������NO2Ϊ3mol����Ӧ4NO2+O2+2H2O=4HNO3���ĵ����������Ϊ7mol���跴Ӧ���ĵ�����Ϊy���������ĵ�NO2Ϊ4y����5y=7mol��y=1.4mol������ʱ����Ϊ1.4mol��V��NO2��=8.6mol��
��������������Ϊ8.6molNO2��1.4molO2������֮��Ϊ8.6mol��46g/mol+1.4mol��32g/mol=440.4g��ƽ��Ħ������
| 440.4g |
| 10mol |
�ʴ�Ϊ��42.08��44.04��
���������⿼���Ϊ�ۺϣ���Ŀ�Ѷ��еȣ�ע���Ʊ������ʵ��װ�úͷ�Ӧԭ���Լ�NO2��O2��H2O��Ӧ�ļ��㣬�������ʵ���Ҫ���ʣ�ע�ػ���֪ʶ�Ļ��ۣ�

��ϰ��ϵ�д�
�����Ŀ