题目内容
对下列事实的解释错误的是
| A.在蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 |
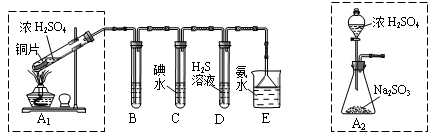
| B.浓H2SO4和Cu加热反应,表现浓H2SO4的强氧化性和酸性 |
| C.常温下,浓硫酸可以用铝罐贮存,说明铝与浓H2SO4不反应 |
| D.蓝色硫酸铜晶体加入浓H2SO4后变白,说明浓H2SO4具有吸水性 |
C
蔗糖中无水分子,浓H2SO4使蔗糖中的氢、氧元素按水的组成脱去,即为脱水性,故A正确;生成二氧化硫,说明浓硫酸表现氧化性(+6价降低到+4价),铜是不活泼金属,能反应,说明浓H2SO4有强氧化性;生成硫酸铜(盐)和水,表现浓H2SO4的酸性;故B正确;
常温下,铝与浓H2SO4发生钝化,即在表面生成致密的氧化膜,阻止内部金属继续反应,故C错误;CuSO4.5H2O(蓝色晶体)失水变成CuSO4(白色粉末),说明浓H2SO4具有吸水性,故D正确
常温下,铝与浓H2SO4发生钝化,即在表面生成致密的氧化膜,阻止内部金属继续反应,故C错误;CuSO4.5H2O(蓝色晶体)失水变成CuSO4(白色粉末),说明浓H2SO4具有吸水性,故D正确

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目