��Ŀ����
X��Y��Z��M��Q�����ֶ���������Ԫ�أ�ԭ�������������� X��Y���γ�����ܼ���X��Y��Z��Ϧ�������֮��Ϊ8��Y��M�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ2.86g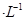 ����ش��������⣺
����ش��������⣺
��1��Y��Z��M����Ԫ��ԭ�Ӱ뾶��С�����˳��Ϊ��дԪ�ط��ţ�________________��
��2��Q�����ڱ��е�λ����____________��
��3��X��Y��Q����Ԫ�ء��γɵ���ԭ�ӷ��ӽṹʽΪ______________��M��QԪ���γɵ�����������Ӧ��ˮ�����н�ǿ�����ǣ�д��ѧʽ��_____________��
��4��Y��Z�γɵĻ�����A�Ⱥ����Ӽ��ֺ����ۼ�,A�ĵ���ʽΪ______________________��
��A����ʢ�з�̪��Һ���Թ��й۲쵽������Ϊ_________________________________��������Ӧ�Ļ�ѧ����ʽΪ_________________��
��5����������װ�ÿɽ�������MY2ת��Ϊ��Ҫ����ԭ��H2MY4���缫a�Ĵ������淢���ĵ缫��Ӧ����ʽΪ__________________________________��������ͨ��MY2��O2�����ʵ�����ѱ�ֵΪ________________��
��1��H,O,Cl,S,Na����2���������ڣ���VIIA�塣��3��H-O-Cl��HClO4����4�� ����Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��SO2 + 2H2O -2e- = SO42- + 4H+��2��1��
����Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��SO2 + 2H2O -2e- = SO42- + 4H+��2��1��
�������������X��Y��Z��M��Q�����ֶ���������Ԫ�أ�ԭ�������������� X��Y���γ�����ܼ���Ϊˮ���ӣ���֪X��Y�ֱ�Ϊ�����Ԫ�ء���������Ϧ�������֮��Ϊ8���Ƶ�ZΪ�ơ�Y��M�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ2.86g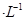 ������Է�������Ϊ64����֪MΪ��Ԫ�أ������Ƕ�����Ԫ�أ�QԪ�ص�ԭ��������M�Ĵ��Ƶ�QΪ�ȡ���1��Y��Z��M����Ԫ��ԭ�Ӱ뾶��С�����˳��Ϊ��дԪ�ط��ţ�H,O,Cl,S,Na����2��Q�����ڱ��е�λ���ǵ������ڣ���VIIA�塣��3��X��Y��Q����Ԫ�ء��γɵ���ԭ�ӷ����Ǵ����ᣬ�ṹʽΪH-O-Cl��M��QԪ���γɵ������������Cl2O7�����Ӧ��ˮ�����н�ǿ�����Ǹ����ᣬ��ѧʽΪHClO4����4��Y��Z�γɵĻ�����A�ǹ������ƣ��Ⱥ����Ӽ��ֺ����ۼ�,A�ĵ���ʽΪ
������Է�������Ϊ64����֪MΪ��Ԫ�أ������Ƕ�����Ԫ�أ�QԪ�ص�ԭ��������M�Ĵ��Ƶ�QΪ�ȡ���1��Y��Z��M����Ԫ��ԭ�Ӱ뾶��С�����˳��Ϊ��дԪ�ط��ţ�H,O,Cl,S,Na����2��Q�����ڱ��е�λ���ǵ������ڣ���VIIA�塣��3��X��Y��Q����Ԫ�ء��γɵ���ԭ�ӷ����Ǵ����ᣬ�ṹʽΪH-O-Cl��M��QԪ���γɵ������������Cl2O7�����Ӧ��ˮ�����н�ǿ�����Ǹ����ᣬ��ѧʽΪHClO4����4��Y��Z�γɵĻ�����A�ǹ������ƣ��Ⱥ����Ӽ��ֺ����ۼ�,A�ĵ���ʽΪ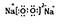 ������������ˮ��Ӧ�������������ƺ������⣬����������Ư���ԣ��ʽ�A����ʢ�з�̪��Һ���Թ��й۲쵽������Ϊ��Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��������MY2�Ƕ�������ת��Ϊ��Ҫ����ԭ��H2MY4�����ᣬ��ͼ��֪�缫a����ʧ���ӣ��缫��Ӧ����ʽΪSO2 + 2H2O -2e- = SO42- + 4H+�����ݵ�ʧ�����غ㣬������ͨ��MY2��O2�����ʵ�����ѱ�ֵΪ2��1��
������������ˮ��Ӧ�������������ƺ������⣬����������Ư���ԣ��ʽ�A����ʢ�з�̪��Һ���Թ��й۲쵽������Ϊ��Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��������MY2�Ƕ�������ת��Ϊ��Ҫ����ԭ��H2MY4�����ᣬ��ͼ��֪�缫a����ʧ���ӣ��缫��Ӧ����ʽΪSO2 + 2H2O -2e- = SO42- + 4H+�����ݵ�ʧ�����غ㣬������ͨ��MY2��O2�����ʵ�����ѱ�ֵΪ2��1��
���㣺���⿼��Ԫ�����ڱ���Ԫ�ص��ƶϣ�����ʽ����д���绯ѧ�е缫��Ӧʽ����д��

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д��±�ΪԪ�����ڱ���һ���֣������Ԫ�آ�~���ڱ��е�λ�ã��û�ѧ����ش��������⣺
| ���� | ��A | | 0 | |||||
| 1 | �� | ��A | ��A | ��A | ��A | ��A | ��A | |
| 2 | | | | �� | �� | �� | | |
| 3 | �� | | �� | | | �� | �� | |
��1���뻭��Ԫ�آ����ӽṹʾ��ͼ�� ��
��2��Ԫ�آ�������������������ȵ�ͬλ�ط����ǣ� ��
��3���ܡ��ݡ��ߵ����Ӱ뾶�ɴ�С��˳��Ϊ�� ��
��4���ڵ�����������Ӧˮ����ĵ��뷽��ʽΪ�� ��
��5���ܡ�������Ԫ�ص�ԭ�Ӱ�1:1��ɵij���������ĵ���ʽΪ�� ��
��6���ɱ�������Ԫ���γɵ�5��10���ӷ��ӳ���ȼ�ϵ�ص�ȼ�ϣ��õ���ڼ��������µĸ�����ӦʽΪ�� ��
��7���ɱ�������Ԫ���γɵ��⻯��A��B������18�����ӣ�A��һ��6ԭ�ӷ��ӣ��������������ȼ�ϣ�B��һ�ֳ���ǿ����������֪16gҺ̬A��Һ̬B��ַ�Ӧ����һ��Һ̬10���ӷ��Ӻ�һ����̬���ʣ����ų�838kJ������д��A��B��Ӧ���Ȼ�ѧ����ʽ�� ��
�о����ʵ��۽ṹ�������������������ʱ仯�ı��ʡ���ش��������⣺
��1��C��Si��NԪ�صĵ縺���ɴ�С��˳����___________________��
C60�ͽ��ʯ����̼��ͬ�������壬������ȣ��۵�ߵ���________��ԭ����____________________________��
��2��A��B��Ϊ�����ڽ���Ԫ�أ����ݱ������ݣ�д��B�Ļ�̬ԭ�ӵĵ����Ų�ʽ��________________��
| ������/��kJ��mol��1�� | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
��3�����ɽ���������ˮ�����γɵ�������Ƿ�����ɫ������d��������Ų��йء�һ��أ�d0��d10�Ų�����ɫ��d1��d9�Ų�����ɫ����[Co��H2O��6]2���Էۺ�ɫ���ݴ��жϣ�[Mn��H2O��6]2��________����ޡ����С�����ɫ��
��4������CO���Ժϳɻ���ԭ��COCl2�������Fe��CO��5�ȡ�
��COCl2���ӵĽṹʽΪ
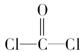 ��ÿ��COCl2�����ں���________���Ҽ���________���м���������ԭ�Ӳ�ȡ________�ӻ������ʽ��
��ÿ��COCl2�����ں���________���Ҽ���________���м���������ԭ�Ӳ�ȡ________�ӻ������ʽ����Fe��CO��5��һ�������·����ֽⷴӦ��Fe��CO��5��s��=Fe��s����5CO��g������Ӧ�����У����ѵĻ�ѧ��ֻ����λ�������γɵĻ�ѧ��������________��
�±��г���A-R 9��Ԫ�������ڱ��е�λ��
| ����\�� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | O |
| 2 | | | | E | | F | | |
| 3 | A | C | D | | | | G | R |
| 4 | B | | | | | | H | |
��1����Ԫ�ط���B D ������B��D������������Ӧ��ˮ����ļ����������� ���ѧʽ����
��2��DԪ�ص�����������Ӧ��ˮ����������������Һ��Ӧ�����ӷ���ʽ�� ��
��3��FԪ���⻯��Ļ�ѧʽ�� �����⻯���ڳ����¸�GԪ���γɵĵ��ʷ�����Ӧ�Ļ�ѧ����ʽ�� ��
��4��GԪ�غ�HԪ�����ߺ˵����֮���� ��
X��Y��Z��W��Ԫ�����ڱ���ǰ30��Ԫ�أ���ԭ���������������������Ϣ���±���
| Ԫ�� | �����Ϣ |
| X | Xԭ�ӻ�̬ʱ���������������ڲ����������2�� |
| Y | Y�Ļ�̬ԭ�����������Ų�ʽΪnsnnpn+2 |
| Z | ZԪ�ص���������븺�۴�����Ϊ6 |
| W | W��̬ԭ��δ�ɶԵ�������ǰ30��Ԫ�������� |
��1��Wλ��Ԫ�����ڱ��� ���ڵ� �壬���̬ԭ��������� �����ӡ�
��2��X�ĵ�һ�����ܱ�Y�� �����С������1mol X22-�к��е�
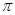 ����ĿΪ ��
����ĿΪ ����3��X��Y����̬�⻯���У����ȶ����� ��д��ѧʽ��,Y��ͬ��Ԫ�أ�����Y��������⻯���зе���͵��� ��
��4��д��KZY3��HZŨ��Һ��Ӧ��ȡZ2�Ļ�ѧ����ʽ�����������ת�Ƶķ������Ŀ ��
��5����֪��X(s)+Y2(g)=XY2(g) ��H 1= ��393.5 kJ?mol��1
XY(g) +1/2Y2(g)=XY2(g) ��H 2= ��282.9 kJ?mol��1
��X(s)��Y2(g)��Ӧ����XY(g)���Ȼ�ѧ��Ӧ����ʽΪ ��