题目内容
由二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同.则该混合气体中二氧化碳、氢气、一氧化碳的体积比可能为( )
分析:同温同压下,密度之比等于相对分子质量之比,同温同压下,混合气体与氮气的密度相同,则混合气体的平均相对分子质量为28,一氧化碳的相对分子质量为28,所以二氧化碳与氢气的平均相对分子质量为28,与一氧化碳的含量无关.根据十字交叉法计算二氧化碳与氢气比例关系.
解答:解:同温同压下,混合气体与氮气的密度相同,则混合气体的平均相对分子质量为28,一氧化碳的相对分子质量为28,所以二氧化碳与氢气的平均相对分子质量为28,根据十字交叉法计算二氧化碳与氢气比例关系.

所以二氧化碳与氢气的体积比为26:16=13:8.
一氧化碳的相对分子质量为28,所以与一氧化碳的含量无关,满足二氧化碳与氢气的体积比为26:16=13:8即可.
故选:BD.

所以二氧化碳与氢气的体积比为26:16=13:8.
一氧化碳的相对分子质量为28,所以与一氧化碳的含量无关,满足二氧化碳与氢气的体积比为26:16=13:8即可.
故选:BD.
点评:考查阿伏伽德罗定律及推论、混合物的有关计算,难度较大,注意利用平均相对分子质量判断化合物的组成.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目

 )是重要的能源物质,研究甲醇具有重要意义。
)是重要的能源物质,研究甲醇具有重要意义。 可制取甲醇,其反应为:
可制取甲醇,其反应为: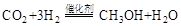

 的
的  晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应为 。
离子。电池工作时正极反应为 。
 氧化成
氧化成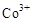 ,然后以
,然后以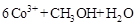
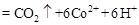 ,该过程中被氧化的元素是 ,当产生标准状况下2.24L
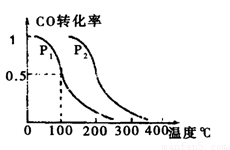
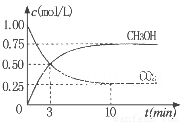
,该过程中被氧化的元素是 ,当产生标准状况下2.24L CH3OH(g)在容积为1L。的密闭容器中分别充入1molCO和2molH2,实验测得甲醇的物质的量和温度、时间的关系曲线如图所示。则该正反应的△H_______0(填“<”、“>”或“=”),判断的理由是______。
CH3OH(g)在容积为1L。的密闭容器中分别充入1molCO和2molH2,实验测得甲醇的物质的量和温度、时间的关系曲线如图所示。则该正反应的△H_______0(填“<”、“>”或“=”),判断的理由是______。
 CH3OH+H2O。
CH3OH+H2O。
 CO(g)+2H2(g)设在容积为2.0L的密闭容器中充入0. 60
molCH3OH(g),体系压强为P1,在一定条件下达到平衡时,体系压强为P2,且P2/P1
=2.2,则该条件下CH3OH 的平衡转化率为______ 。
CO(g)+2H2(g)设在容积为2.0L的密闭容器中充入0. 60
molCH3OH(g),体系压强为P1,在一定条件下达到平衡时,体系压强为P2,且P2/P1
=2.2,则该条件下CH3OH 的平衡转化率为______ 。

 CH3OH(g)
CH3OH(g)