题目内容
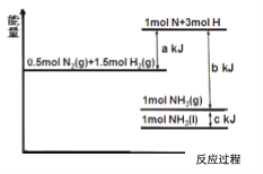
【题目】I、根据能量变化示意图,请写出氮气和氢气合成液态 的氨气的热化学方程式_____;
Ⅱ、已知:NO2(g)+ SO2(g)![]() SO3(l)+ NO(g)ΔH=-51.5kJ·mol-1
SO3(l)+ NO(g)ΔH=-51.5kJ·mol-1
若在一定条件下,将 NO2 与 SO2 以体积比 1:2 置于恒容密闭容器 中发生上述反应,
①下列能说明反应达到平衡状态的是_____。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3 和 NO 的物质的量之比保持不变 d.每消耗 1 mol SO3 的同时生成 1 molNO2
e.容器内气体密度不变
②恒容密闭容器中发生上述反应时,若加入 Ar 气,反 应速率_____(变大、变小或不变)。
【答案】 N2(g)+3H2(g)![]() 2NH3(l)ΔH=2(a-b-c)kJ·molˉ1 abe 不变
2NH3(l)ΔH=2(a-b-c)kJ·molˉ1 abe 不变
【解析】试题分析:I、反应的焓变=生成物的总能量-反应物的总能量;Ⅱ、①根据平衡标志分析;②恒容密闭容器中发生上述反应时,若加入Ar气,反应体系中气体浓度不变;
解析:I、反应的焓变=生成物的总能量-反应物的总能量;氮气和氢气合成液态的氨气的热化学方程式N2(g)+3H2(g) ![]() 2NH3(l) ΔH=2(a-b-c)kJ·molˉ1;Ⅱ、①a.根据方程式,反应前后气体物质的量改变,所以压强是变量,体系压强保持不变一定平衡,故a正确; b.混合气体颜色保持不变,说明NO2浓度不变,一定达到平衡状态,故b正确; c.反应过程中SO3 和 NO 的物质的量之比始终是1:1,所以SO3 和 NO 的物质的量之比保持不变不一定达到平衡状态,故c错误; d.每消耗 1 mol SO3 的同时生成 1 molNO2,都是指逆反应,故d不一定平衡,d错误; e.根据
2NH3(l) ΔH=2(a-b-c)kJ·molˉ1;Ⅱ、①a.根据方程式,反应前后气体物质的量改变,所以压强是变量,体系压强保持不变一定平衡,故a正确; b.混合气体颜色保持不变,说明NO2浓度不变,一定达到平衡状态,故b正确; c.反应过程中SO3 和 NO 的物质的量之比始终是1:1,所以SO3 和 NO 的物质的量之比保持不变不一定达到平衡状态,故c错误; d.每消耗 1 mol SO3 的同时生成 1 molNO2,都是指逆反应,故d不一定平衡,d错误; e.根据![]() ,气体质量是变量,体积是恒量,所以密度是变量,容器内气体密度不变一定达到平衡状态,故e正确;②恒容密闭容器中发生上述反应时,若加入Ar气,反应体系中气体浓度不变,所以反应速率不变。
,气体质量是变量,体积是恒量,所以密度是变量,容器内气体密度不变一定达到平衡状态,故e正确;②恒容密闭容器中发生上述反应时,若加入Ar气,反应体系中气体浓度不变,所以反应速率不变。