题目内容
【题目】过氧化钙是一种温和的氧化剂,常温下为白色固体,易溶于酸,难溶于水、乙醇等溶剂。
(1)某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙,按气流方向连接顺序为__________________(填仪器接口的字母编号,装置可重复使用);实验步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入一段时间气体,加热药品;③反应结束后,先想灭酒精灯,待反应管冷却至室温后,停止通入气体;④拆除装置,取出产物。实验步骤③的操作目的是______________________。

(2)利用反应Ca2++H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4+,在碱性环境下制取CaO2·8H2O的装置如下:

①仪器C的名称____________;反应结束后,经__________(填操作名称)、洗涤、低温烘干可获得CaO2·8H2O。
②装置A中发生反应的化学方程式为_____________;装置B中用冰水浴控制温度,其可能原因是______________________________。
③测定产品中CaO2·8H2O的含量的实验步骤如下:
步骤一:准确称取a g产品放入锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴___________(作指示剂)。
步骤三:逐滴加入浓度为c mol/L的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出三次平均消耗Na2S2O3溶液体枳为VmL。则CaO2·8H2O的质量分数为____(用含字母的式子表示)。 [已知:I2+2S2O32-=2I-+ S4O62-]
【答案】 cedabe或cedbac 防止倒吸 分液漏斗 过滤 Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O 温度低可减少过氧化氢分解,提高过氧化氢的利用率(或反应放热,温度低有利于提高产率) 淀粉溶液 [(108cV×10-3)/a]×100%
CaCl2+2NH3↑+2H2O 温度低可减少过氧化氢分解,提高过氧化氢的利用率(或反应放热,温度低有利于提高产率) 淀粉溶液 [(108cV×10-3)/a]×100%
【解析】(1)制备过氧化钙时,用双氧水制备氧气,钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,而制备的氧气中会混有水蒸气,所以在与钙化合之前需要干燥,选用试剂是浓硫酸;同时为防止空气中水蒸气进入,最后还需要连接浓硫酸的洗气瓶,所以正确的顺序为:cedabe或cedbac;实验结束时为防止空气进入装置,还要继续通氧气直到装置冷却,所以实验步骤③的操作目的是防止倒吸;(2)①根据图中仪器可知,仪器C的名称为分液漏斗;反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O;②装置A中利用熟石灰与氯化铵共热制取氨气,发生反应的化学方程式为Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O;装置B中用冰水浴控制温度,其可能原因是温度低可减少过氧化氢分解,提高过氧化氢的利用率(或反应放热,温度低有利于提高产率);③利用淀粉遇碘变蓝,故选择的指示剂为淀粉溶液;(4)根据电子转移守恒关系可知:
CaCl2+2NH3↑+2H2O;装置B中用冰水浴控制温度,其可能原因是温度低可减少过氧化氢分解,提高过氧化氢的利用率(或反应放热,温度低有利于提高产率);③利用淀粉遇碘变蓝,故选择的指示剂为淀粉溶液;(4)根据电子转移守恒关系可知:
CaO2·8H2O~ I2 ~ 2S2O32-
216 2
am c×V×10-3mol
因此m%=![]() 。
。

【题目】(1)某同学为探究酸性KMnO4溶液和H2C2O4(草酸,二元弱酸)溶液的反应过程,进行如下实验。请完成以下问题:
①写出酸性KMnO4溶液和H2C2O4的离子方程式___________________________________。
②配制100mL0.0400mol·L-1的H2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是_______________________________________。
③将KMnO4溶液逐滴滴入一定体积的酸性H2C2O4溶液中(温度相同,并振荡),记录的现象如下:
滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
先滴入第1滴 | 60s |
褪色后,再滴入第2滴 | 15s |
褪色后,再滴入第3滴 | 3s |
褪色后,再滴入第4滴 | 1s |
请分析KMnO4溶液褪色时间变化的可能原因___________________________________。
(2)![]() 和
和![]() 在溶液中可相互转化。室温下,初始浓度为1.0 mol·L-1的Na2CrO4溶液中
在溶液中可相互转化。室温下,初始浓度为1.0 mol·L-1的Na2CrO4溶液中![]() 随c(H+)的变化如图所示
随c(H+)的变化如图所示

①用离子方程式表示溶液中![]() 和
和![]() 的转化反应_________。
的转化反应_________。
②由图可知,溶液酸性减小, ![]() 的平衡转化率_________(填“增大”“减小”或“不变”)。
的平衡转化率_________(填“增大”“减小”或“不变”)。
③升高温度,溶液中![]() 的平衡转化率减小,则该反应的ΔH_________0(填“大于”“小于”或“等于”)。
的平衡转化率减小,则该反应的ΔH_________0(填“大于”“小于”或“等于”)。
【题目】在恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:
2A(g)+B(g)![]() 2C(g) ΔH>0。
2C(g) ΔH>0。
达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( )
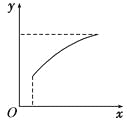
选项 | x | y |
A | 再通入A | B的转化率 |
B | 加入催化剂 | A的体积分数 |
C | 压强 | 混合气体的总物质的量 |
D | 温度 | 混合气体的总物质的量 |



