题目内容
【题目】已知:R﹣CH=CH﹣O﹣R′ ![]() R﹣CH2CHO+R′OH(烃基烯基醚) 烃基烯基醚A的相对分子质量为176,分子中碳氢原子数目比为3:4.与A相关的反应如图:
R﹣CH2CHO+R′OH(烃基烯基醚) 烃基烯基醚A的相对分子质量为176,分子中碳氢原子数目比为3:4.与A相关的反应如图: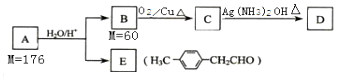
请回答下列问题:
(1)A的分子式为 , B的名称是 .
(2)写出C→D反应的化学方程式: .
(3)链烃M的相对分子质量比B多24,分子中所有碳原子均在同一平面上,其结构简式是 .
【答案】
(1)C12H16O;1﹣丙醇(或正丙醇)
(2)CH3CH2CHO+2Ag(NH3)2OH ![]() CH3CH2COONH4+2Ag↓+3NH3↑+H2O
CH3CH2COONH4+2Ag↓+3NH3↑+H2O
(3)(CH3)2C=C(CH3)2
【解析】解:(1)由上述分析可知,A的分子式为C12H16O,B为CH3CH2CH2OH,名称为1﹣丙醇(或正丙醇),
所以答案是:C12H16O;1﹣丙醇(或正丙醇);(2)C→D反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OH ![]() CH3CH2COONH4+2Ag↓+3NH3↑+H2O,
CH3CH2COONH4+2Ag↓+3NH3↑+H2O,
所以答案是:CH3CH2CHO+2Ag(NH3)2OH ![]() CH3CH2COONH4+2Ag↓+3NH3↑+H2O;(3)链烃M的相对分子质量比B多24,则M相对分子质量为84,分子中C原子最大数目=
CH3CH2COONH4+2Ag↓+3NH3↑+H2O;(3)链烃M的相对分子质量比B多24,则M相对分子质量为84,分子中C原子最大数目= ![]() =7,故M为C6H12,分子中所有碳原子均在同一平面上,则分子中含有C=C双键,且不饱和碳原子连接4个甲基,所以M结构简式为(CH3)2C=C(CH3)2,
=7,故M为C6H12,分子中所有碳原子均在同一平面上,则分子中含有C=C双键,且不饱和碳原子连接4个甲基,所以M结构简式为(CH3)2C=C(CH3)2,
所以答案是:(CH3)2C=C(CH3)2.

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色.如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl﹣)生产CuCl的流程: 
根据以上信息回答下列问题:
(1)生产过程中X的化学式为 .
(2)写出产生CuCl的化学方程式: .
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由 . 实际生产中SO2要适当过量,原因可能是(答一点即可).
(4)实验探究pH对CuCl产率的影响如下表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为 , 当pH较大时CuCl产率变低原因是 . 调节pH时,(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是 .
(5)氯化亚铜的定量分析: ①称取样品0.25g和过量的FeCl3溶液于锥形瓶中,充分溶解.
②用0.10molL﹣1硫酸铈标准溶液滴定.已知:CuCl+FeCl3═CuCl2+FeCl2、Fe2++Ce4+═Fe3++Ce3+ . 三次平行实验结果如下(平行实验结果相差不能超过1%):
平行实验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为(结果保留三位有效数字).


