题目内容
【题目】下列离子方程式中,正确的是
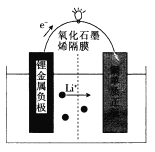
A.用惰性电极电解MgCl2溶液:2Cl-+H2O![]() 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B.碳酸钠溶液显碱性:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
C.氯气通入冷水中:Cl2 +H2O ![]() Cl-+ClO-+2H+
Cl-+ClO-+2H+
D.碳酸镁悬浊液中加醋酸:CO32-+2CH3COOH= 2CH3COO-+CO2↑+H2O
【答案】B
【解析】
A.用惰性电极电解MgCl2溶液的离子反应为Mg2++2Cl-+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑,故A错误;
Mg(OH)2↓+Cl2↑+H2↑,故A错误;
B.碳酸钠溶液显碱性的离子反应为CO32-+H2O![]() HCO3-+OH-,故B正确;
HCO3-+OH-,故B正确;
C.氯气通入冷水中的离子反应为Cl2+H2O![]() Cl-+HClO+H+,故C错误;
Cl-+HClO+H+,故C错误;
D.碳酸镁悬浊液中加醋酸的离子反应为MgCO3+2CH3COOH=2CH3COO-+CO2↑+H2O+Mg2+,故D错误;
故答案为B。

 阅读快车系列答案
阅读快车系列答案【题目】甲、乙两同学为探究![]() 与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
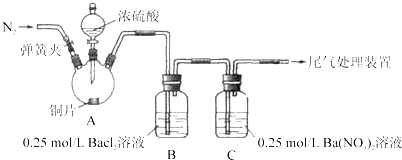
实验操作和现象:
操作 | 现象 |
关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上放略显浅棕色并逐渐消失 |
打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
从B、C中分别取少量白色沉淀,加稀盐酸 | 尚未发现白色沉淀溶解 |
(1)A中反应的化学方程式是_________________。
(2)C中白色沉淀是_______,该沉淀的生成表明SO2具有_______性。
(3)C中液面上方生成浅棕色气体的化学方程式是______。
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①未证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是____;乙在A、B间增加洗气瓶D,D中盛放的试剂是______。
②进行实验,B中现象:
甲 | 大量白色沉淀 |
乙 | 少量白色沉淀 |
检验白色沉淀,发现均不溶于稀盐酸。结合离子方程式解释实验现象异同的原因:___。
(5)合并(4)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是_____。