��Ŀ����
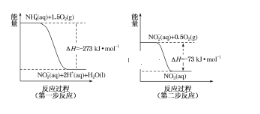
����Ŀ��������Fe/Ni���ϲ�����ȥ����Ⱦˮ���NO3-��Ni�����뷴Ӧ�������ڲ��ϱ���Ļ���λ������������Ӧ������λ�㱻����������ռ�ݻᵼ�����ʼ���(NH4+��ռ�ݻ���λ��)����Ӧ������ͼ��ʾ��
��1�����Ի����У�����Fe/Niȥ��NO3-��������������ii����������
��.NO3-+Fe+2H+=NO2-+Fe2++H2O
��.___+___+___H+=___Fe2++___+___
��2����ʼpH=2.0�ķ�Һ��Ӧ15min���ִ�����ɫ��״����˺�ܿ��ɺ��ɫ����ϻ�ѧ������������仯���̵�ԭ��___��
��3��ˮ���ʼpH��Ӱ�췴Ӧ���ʣ���ͬpH����������Һ������Fe/Ni��Ӧʱ����Һ��![]() ��ʱ��ı仯��ͼ1��ʾ��(ע��c0(NO3-)Ϊ��ʼʱNO3-��Ũ�ȡ�)
��ʱ��ı仯��ͼ1��ʾ��(ע��c0(NO3-)Ϊ��ʼʱNO3-��Ũ�ȡ�)

��Ϊ�ﵽ���ȥ���ʣ�Ӧ��ˮ��ij�ʼpH=___��
��t<15min��pH=2.0����Һ��Ӧ������죬t>15min���䷴Ӧ����Ѹ�ٽ��ͣ�ԭ��ֱ���___��
��4���ܵ���ָ��Һ�������ƶ������к�����Ũ��֮�ͣ�����Fe/Ni����ijŨ����������Һʱ����ʱ��ı仯��ͼ2��ʾ��40minʱ�ܵ����ϳ�ʼʱ�½������ܵ�ԭ����___��

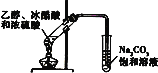
��5�����õ����������ˮ���е�NO3-����������N2�ݳ�����װ�ü�ת��ͼ��ͼ��ʾ��
�������ĵ缫��ӦʽΪ___��
������N2�����ӷ���ʽΪ___��

���𰸡�NO2- 3Fe 8 3 NH4+ 2H2O )Fe2+��ˮ�з���ˮ�⣬Fe2++2H2OFe(OH)2+2H+�����ŷ�Ӧ���У�c(H+)��С��ƽ�����ƣ�����Fe(OH)2������֮������Ӧ4Fe(OH)2+O2+2H2O=4Fe(OH)3����ɺ��ɫ��Fe(OH)3 6.5 pH=2����Һ�У�t<15minʱ����Һ��H+Ũ�Ƚϸߣ���˷�Ӧ���ʽϿ죬��Һ�в���Fe2+��pH�������ʽϿ죬t>15minʱ����������Fe(OH)2�������ڻ���λ���ϣ���С�Ӵ��������˷�Ӧ����Ѹ���½� ��Ӧ������H+�����ģ���ҺpH���ߣ�t=40minʱ����Һ�к�N������Ҫ��NH4+����ʽ���ڣ�һ����NH4+����NH3�ݳ�(��Ӧ������NO2-��Fe��ԭ����N2�ݳ�) NO3-+8e-+10H+=NH4++3H2O 2NH4++3HClO=N2��+3Cl-+5H++3H2O
��������
��1������ͼ��֪�����Ի����У�����![]() ȥ��
ȥ��![]() ��������
��������![]() �������㱻Fe��ԭΪ
�������㱻Fe��ԭΪ![]() ��
��![]() ��
��![]() ������������㱻Fe��ԭΪ
������������㱻Fe��ԭΪ![]() ��
��![]() ��
��
��2����ʼpH=2.0�ķ�Һ��Ӧ15min���ִ�����ɫ��״����˺�ܿ��ɺ��ɫ���������������������е���������Ϊ����������
��3���������ͼ����Ϣ���жϵ���pHΪ���ٵ�ʱ��ȥ���ʽϸߣ���ν��ͷ�Ӧ���ʱ�����
��5���缫����ʽ��д����������Ϣ�ж�����������ԭ��Ӧ��NO3-��ԭN2��![]() ��
��
![]() ����ͼ��֪�����Ի����У�����
����ͼ��֪�����Ի����У�����![]() ȥ��
ȥ��![]() ��������
��������![]() �������㱻Fe��ԭΪ
�������㱻Fe��ԭΪ![]() ��
��![]() ��
��![]() ������������㱻Fe��ԭΪ
������������㱻Fe��ԭΪ![]() ��
��![]() ��
��
�ʴ�Ϊ��![]() ��3Fe��8��3��
��3Fe��8��3��![]() ��
��![]() ��
��
![]() ��ʼ
��ʼ![]() �ķ�Һ��Ӧ15min���ִ�����ɫ��״����˺�ܿ��ɺ��ɫ����Ϊ
�ķ�Һ��Ӧ15min���ִ�����ɫ��״����˺�ܿ��ɺ��ɫ����Ϊ![]() ��ˮ�з���ˮ�⣬
��ˮ�з���ˮ�⣬![]() �����ŷ�Ӧ���У�
�����ŷ�Ӧ���У�![]() ��С��ƽ�����ƣ�����
��С��ƽ�����ƣ�����![]() ������֮������Ӧ
������֮������Ӧ![]() ����ɺ��ɫ��
����ɺ��ɫ��![]() ��
��
�ʴ�Ϊ��![]() ��ˮ�з���ˮ�⣬
��ˮ�з���ˮ�⣬![]() �����ŷ�Ӧ���У�
�����ŷ�Ӧ���У�![]() ��С��ƽ�����ƣ�����
��С��ƽ�����ƣ�����![]() ������֮������Ӧ
������֮������Ӧ![]() ����ɺ��ɫ��
����ɺ��ɫ��![]() ��
��
![]() ����ͼ��֪
����ͼ��֪![]() ʱ����Ӧ��죬ȥ������ߣ���Ϊ�ﵽ���ȥ���ʣ�Ӧ��ˮ��ij�ʼ
ʱ����Ӧ��죬ȥ������ߣ���Ϊ�ﵽ���ȥ���ʣ�Ӧ��ˮ��ij�ʼ![]() ��
��
�ʴ�Ϊ��![]() ��
��
![]() ����Һ�У�
����Һ�У�![]() ʱ����Һ��
ʱ����Һ��![]() Ũ�Ƚϸߣ���˷�Ӧ���ʽϿ죬��Һ�в���
Ũ�Ƚϸߣ���˷�Ӧ���ʽϿ죬��Һ�в���![]() ��pH�������ʽϿ죬��
��pH�������ʽϿ죬��![]() ��
��![]() ����Һ��Ӧ������죬
����Һ��Ӧ������죬
![]() ʱ����������
ʱ����������![]() �������ڻ���λ���ϣ���С�Ӵ��������˷�Ӧ����Ѹ���½�����
�������ڻ���λ���ϣ���С�Ӵ��������˷�Ӧ����Ѹ���½�����![]() ���䷴Ӧ����Ѹ�ٽ��ͣ�
���䷴Ӧ����Ѹ�ٽ��ͣ�
�ʴ�Ϊ��![]() ����Һ�У�
����Һ�У�![]() ʱ����Һ��
ʱ����Һ��![]() Ũ�Ƚϸߣ���˷�Ӧ���ʽϿ죬��Һ�в���
Ũ�Ƚϸߣ���˷�Ӧ���ʽϿ죬��Һ�в���![]() ��pH�������ʽϿ죬
��pH�������ʽϿ죬![]() ʱ����������
ʱ����������![]() �������ڻ���λ���ϣ���С�Ӵ��������˷�Ӧ����Ѹ���½���
�������ڻ���λ���ϣ���С�Ӵ��������˷�Ӧ����Ѹ���½���
![]() ʱ�ܵ����ϳ�ʼʱ�½����ܵ�ԭ��Ϊ����Ӧ������
ʱ�ܵ����ϳ�ʼʱ�½����ܵ�ԭ��Ϊ����Ӧ������![]() �����ģ���ҺpH���ߣ�
�����ģ���ҺpH���ߣ�![]() ʱ����Һ�к�N������Ҫ��
ʱ����Һ�к�N������Ҫ��![]() ����ʽ���ڣ�һ����
����ʽ���ڣ�һ����![]() ����
����![]() �ݳ�
�ݳ�![]() ��Ӧ������
��Ӧ������![]() ��Fe��ԭ����
��Fe��ԭ����![]() �ݳ�
�ݳ�![]() ��
��
�ʴ�Ϊ����Ӧ������![]() �����ģ���ҺpH���ߣ�
�����ģ���ҺpH���ߣ�![]() ʱ����Һ�к�N������Ҫ��
ʱ����Һ�к�N������Ҫ��![]() ����ʽ���ڣ�һ����
����ʽ���ڣ�һ����![]() ����
����![]() �ݳ�
�ݳ�![]() ��Ӧ������
��Ӧ������![]() ��Fe��ԭ����
��Fe��ԭ����![]() �ݳ�
�ݳ�![]() ��
��
![]() ����������ԭ��Ӧ��Ԫ�ػ��ϼ۽��ͣ���Ϊ
����������ԭ��Ӧ��Ԫ�ػ��ϼ۽��ͣ���Ϊ![]() �õ���������
�õ���������![]() ���ʵ缫��ӦΪ��
���ʵ缫��ӦΪ��![]() ��
��
�ʴ�Ϊ��![]() ��
��
![]() ��ͼ��֪���������������ɵ�
��ͼ��֪���������������ɵ�![]() ��HClO��Ӧ���ã���Ԫ�ػ��ϼ����ߣ�����Ԫ�ػ��ϼ۽������������ӣ��ʷ�ӦΪ��
��HClO��Ӧ���ã���Ԫ�ػ��ϼ����ߣ�����Ԫ�ػ��ϼ۽������������ӣ��ʷ�ӦΪ��![]() ��
��
�ʴ�Ϊ��![]() ��
��

 Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д� ������������Ծ�ϵ�д�
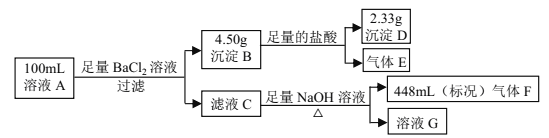
������������Ծ�ϵ�д�����Ŀ��ƽ�������ʾ�����������л���������ķϲ�����ĩ(��SiO2��Fe2O3��CeO2)�����÷ϲ�����ĩ������ȡ���ֻ�����Ʒ�������������:

�������Ͽ�֪:
��CeO2����:���ƻ�ƺ�ɫ��ĩ��������ˮ�ͼ������;��ǿ�����ԡ�
��Ce3+�ڼ����̼������Һ���������ܵ�̼�Ḵ��Ce2(CO3):Na2CO3��2H2O��
�۳���ʱ���ֳ�������ܶȻ�����:
������ | Fe(OH)3 | Ce(OH)3 |
Ksp | 4.0��10-38 | 1.5��10-20 |
�ش���������:
(1)���̢ٷ���������õ��IJ���������_______________________________��
(2)���̢��з�����Ӧ�����ӷ���ʽΪ_________________________________�����̢��з����Ļ�ѧ��Ӧ����ʽΪ__________________________________��
(3)��ƷI��һ�����͡���ɫ�Ķ�ܾ�ˮ���������������������������������������������Ϊһ�塣��ˮ�����У�Na2FeO4 ���������������õ�ԭ����_________________��
(4)��ҵ��Ҳ���õ��ŨNaOH��Һ�Ʊ���ƷI���������缫��д�����ʱ���������ĵ缫��Ӧ����ʽ_________________��
(5)���������У���ij������Ũ�Ƚ���10��5 mol��L-1ʱ������Ϊ��������ȫ���������̢���Fe3+������ȫʱ��Һ��pH=_____ (��֪ lg2=0.3)��
(6)д����ƷIII��һ����;______________________________________��