题目内容
将a g氯酸钾充分加热分解(同时加入少量MnO2),得到标准状况下b L气体,残留物充分溶解后所得溶液中共有c个溶质离子。则阿伏加德罗常数(NA)可表示为
A.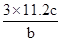 | B.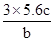 | C.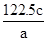 | D.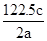 |
BD
试题分析:氯酸钾受热分解的化学方程式是:2KClO3
 2KCl+3O2↑n(KClO3)=(a÷122.5)mol; n(O2) ="V/Vm=" (b÷22.4)mol,n(KCl)=c÷2NAmol. n(KClO3): n(KCl): n(O2)="2:2:3." a÷122.5=c÷2NA,解得NA=
2KCl+3O2↑n(KClO3)=(a÷122.5)mol; n(O2) ="V/Vm=" (b÷22.4)mol,n(KCl)=c÷2NAmol. n(KClO3): n(KCl): n(O2)="2:2:3." a÷122.5=c÷2NA,解得NA=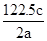 。(c÷2NA):(b÷22.4)=2:3解得NA=
。(c÷2NA):(b÷22.4)=2:3解得NA=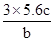 故选项为BD。
故选项为BD。
练习册系列答案
相关题目
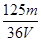 mol/L
mol/L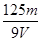 mol/L
mol/L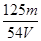 mol/L
mol/L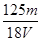 mol/L
mol/L