题目内容
【题目】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为_________
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤
步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。
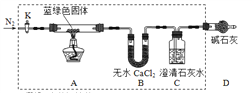
请回答下列问题:
(1)假设2中的沉淀为___________________。
(2)假设1中沉淀为Cu(OH)2的理论依据是(用离子方程式表示)____________。
(3)无水乙醇洗涤的目的_______________________________________。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明___________成立。(填写“假设1” “假设2”或“假设3”)。
(5)乙同学认为只要将上图中B装置的试剂改用______试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是_______________________。
【答案】 CuCO3 Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑ 使产物在常温下更易于干燥 假设1 无水CuSO4 A中蓝绿色固体变黑色,B中固体变蓝,C中有白色沉淀产生
【解析】(1)根据假设1和假设3可以得到:假设2为沉淀是CuCO3 。
(2)假设1中沉淀为Cu(OH)2的原因是,碳酸钠溶液水解显碱性,氢氧根离子和铜离子反应生成氢氧化铜沉淀,所以离子反应方程式为:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑。
(3)无论是氢氧化铜还是碳酸铜,受热都易分解,所以不能烘干,使用无水乙醇洗涤的目的是为了将沉淀表面的水洗去,而乙醇的挥发性原好于水,这样使产物在常温下更易于干燥。
(4)C中无明显现象,说明未生成二氧化碳,即沉淀中不存在碳元素,所以假设1成立。
(5)氢氧化铜受热分解得到水蒸气,碳酸铜受热分解得到二氧化碳,所以验证以上所有假设,应该要验证水蒸气和二氧化碳气体,验证水蒸气应该用无水硫酸铜,所以应该将B中固体换成无水硫酸铜。
(4)B中固体换成无水硫酸铜后,若假设3成立,则分解应该得到氧化铜、水蒸气和二氧化碳气体,所以看到的现象是:A中蓝绿色固体变黑色,B中固体变蓝,C中有白色沉淀产生。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案【题目】已知合成氨反应的浓度数据如下,当用氨气浓度的增加来表示该化学反应速率时,其速率为( )
N2+3H22NH3 | |||
起始浓度mol/L | 1.0 | 3.0 | 0 |
2秒末浓度mol/L | 0.6 | 1.8 | a |
A.0.2mol/(Ls)
B.0.4mol/(Ls)
C.0.6mol/(Ls)
D.0.8mol/(Ls)