题目内容
【题目】2011年下半年,我省第一条横跨湘江的过江隧道将建成通车,在工程建设中用量最大的硅酸盐材料是( )
A.钢筋B.水泥C.铝合金D.陶瓷
【答案】B
【解析】
建设隧道用的主要材料是钢筋和混凝土,据此分析判断。
A.钢筋属于金属材料,不是硅酸盐材料,故A错误;
B.水泥是混凝土的主要成分,属于硅酸盐材料,故B正确;
C.铝合金属于金属材料,不是硅酸盐材料,故C错误;
D.陶瓷属于硅酸盐材料,但是在建设隧道时用量不大,故D错误;
故选B。

【题目】已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生氧化还原反应。甲、乙两个实验小组欲探究影响化学反应速率的因素,设计实验方案如下(实验中所用KMnO4溶液均已酸化)
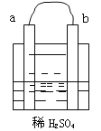
(1)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率,实验装置如图所示:

实验时仪器中的A溶液一次性加入,A、B的成分见下表:
序号 | A溶液 | B溶液 |
① | 2 mL 0.1 mol·L-1H2C2O4溶液 | 4 mL 0.01 mol·L-1KMnO4溶液 |
② | 2 mL 0.2 mol·L-1H2C2O4溶液 | 4 mL 0.01 mol·L-1KMnO4溶液 |
③ | 2 mL 0.2 mol·L-1H2C2O4溶液 | 4 mL 0.01 mol·L-1KMnO4溶液,少量MnSO4固体(催化剂) |
①盛放A溶液的仪器名称_______,锥形瓶中反应的化学方程式:______
②该实验探究的是_____因素对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是____(填实验序号)。
(2)乙组:通过测定KMnO4溶液褪色所需时间的长短来比较化学反应速率。
取两支试管各加入2 mL 0.1 mol·L-1H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol·L-1KMnO4溶液,将四支试管分成两组(每组各有一支试管盛有H2C2O4溶液和KMnO4溶液),一组放入冷水中,另一组放入热水中,一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验试图探究________因素对化学反应速率的影响,但该组同学始终没有看到溶液完全褪色,其原因是______
【题目】下表为元素周期表的一部分,参照元素![]() 在表中的位置,按要求回答下列问题:
在表中的位置,按要求回答下列问题:
周期主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ⅧA |
一 |
| |||||||
二 |
|
|
| |||||
三 |
|
|
|
|
|
(1)在元素![]() ,最活泼的金属元素是______
,最活泼的金属元素是______![]() 填元素名称
填元素名称![]() ;最活泼的非金属元素名称是______
;最活泼的非金属元素名称是______![]() 填元素名称
填元素名称![]()
(2)用电子式表示元素![]() 与
与![]() 形成的原子个数比为1:2的化合物 _______________。元素①和③所形成的化学键的类型是___________________。
形成的原子个数比为1:2的化合物 _______________。元素①和③所形成的化学键的类型是___________________。
(3)![]() 、
、![]() 三种元素的原子半径由大到小的顺序是______
三种元素的原子半径由大到小的顺序是______![]() 用元素符号表示
用元素符号表示![]() 。
。
(4)元素![]() 和
和![]() 所能形成的气态氢化物的稳定性___________
所能形成的气态氢化物的稳定性___________![]() 化学式表示
化学式表示![]() ;元素
;元素![]() 、
、![]() 、
、![]() 的最高价氧化物对应的水化物的酸性由强到弱的顺序 ___
的最高价氧化物对应的水化物的酸性由强到弱的顺序 ___![]() 化学式表示
化学式表示![]()
(5)写出元素![]() 和
和![]() 的最高价氧化物的水化物相互反应的离子方程式:______________。
的最高价氧化物的水化物相互反应的离子方程式:______________。