题目内容
【题目】A、B是前三周期的元素,它们的离子A2-和B3+有相同的电子层结构,下列说法正确的是
A.原子半径A>BB.原子序数A>B
C.离子半径A2—>B3+D.质量数A>B
【答案】C
【解析】
A、B是前三周期的元素,它们的离子A2-和B3+有相同的电子层结构,则A为O、B为Al。
A. 原子半径O<Al,A错误;
B. 原子序数O<Al,B错误;
C. 离子半径O2—>Al3+,C正确;
D. 通常情况下,O的质量数为16、17、18,而Al的质量数为27,质量数A<B,D错误。
答案为C。

 第1卷单元月考期中期末系列答案
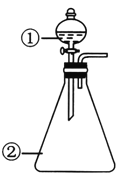
第1卷单元月考期中期末系列答案【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象和结论合理的是
选项 | ①中物质 | ②中的物质 | 预测②中的现象和结论 |
|
A | 浓盐酸 | 二氧化锰 | 立即产生大量黄绿色气体,证明 HC1具有还原性和酸性 | |
B | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色,证明草酸具有还原性 | |
C | 硫酸铝饱和溶液 | 碳酸钠饱和溶液 | 立即产生大量气泡,证明两者相互促进水解 | |
D | 蒸馏水 | 过氧化钠粉末 | 立即产生大量气泡,滴加酚酞溶液后变红,说明过氧化钠是碱性氧化物 |
A. A B. B C. C D. D
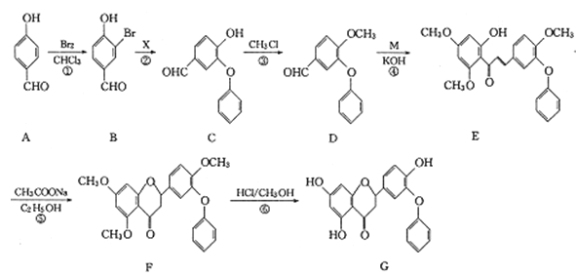
【题目】第二代半导体材料——(Ⅲ-V)A族化合物的特殊性能使之成为科学家的研究热点之一。
(1) 基态镓原子的价电子轨道表示式为_____________。
(2) N、P、As位于同一主族,基态氮原子的核外共有________种不同运动状态的电子,N2O的空间构型为_________,NH4NO3中N的杂化方式为_________________,与PO43-互为等电子体的分子有________________(填一种即可)。
(3)已知NH3分子的键角约为107°,而PH3分子的键角约为94°,试用价层电子对互斥理论解释NH3的键角比PH¥的键角大的原因__________________________。
(4)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有________________。
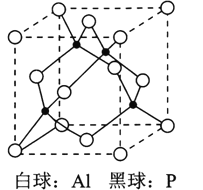
(5)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:
物质 | BN | AIN | GaN |
熔点/℃ | 3000 | 2200 | 1700 |
试从结构的角度分析它们熔点不同的原因_____________________。
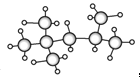
(6)磷化铝晶胞如图所示,A1原子的配位数为________,若两个铝原子之间的最近距离为d pm,NA代表阿伏加德罗常数的值, 则磷化铝晶体的密度ρ=_________g/cm3。