��Ŀ����
����Ŀ���˰�ȫ���������Ⱦ������������������Ĺ㷺���ӡ��ڱ�ը�ĺ˵�վ��Χ���з��������ʵ�131���137����131һ�����������룬���ܻ�������״�ټ�����
��1��Cs(�)�ļ۵����Ų�ʽΪ6s1�����ͬ�����ǰ������(������������)������Ԫ��X��Y��Z�ĵ�һ���������±���
Ԫ�ش��� | X | Y | Z |
��һ������/(kJ��mol��1) | 520 | 496 | 419 |
��������Ԫ��X��Y��Z��Ԫ�ط��ŷֱ�Ϊ________����̬Zԭ�ӵĺ�������Ų�ʽΪ________��X�γɵĵ��ʾ����к��еĻ�ѧ��������________��
��2��F��Iͬ���壬BeF2��H2O����������ԭ�ӹ��ɵĹ��ۻ�������ӣ����߷����е�����ԭ��Be��O���ӻ���ʽ�ֱ�Ϊ________��________��BeF2���ӵ����幹����________��H2O���ӵ����幹����________��
��3�����ͬ������Ⱦ��к�ǿ�Ļ����ԣ����γɴ����ĺ��Ȼ����BCl3������B��Cl���ļ���Ϊ________��
��4��131I2����ľ����ṹ��ͼ����ʾ���þ����к���________��131I2���ӣ�KI�ľ����ṹ��ͼ����ʾ��ÿ��K������________��I����

�ס��������������� ��
��5��KI������ܶ�Ϊ�� g��cm��3��K��I��Ħ�������ֱ�ΪMK g��mol��1��MIg��mol��1��ԭ�Ӱ뾶�ֱ�ΪrKpm��rIpm�������ӵ�������ֵΪNA����KI������ԭ�ӵ����ռ��������İٷ���Ϊ________��
���𰸡�Li��Na��K1s22s22p63s23p64s1������spsp3ֱ����V��120��46![]() ��100%
��100%
��������
(1)��蘆����������Ų�ʽΪ6s1����֪X��Y��ZΪ����A�壬����A��ǰ�����ڵ�Ԫ�طֱ�ΪH��Li��Na��K�������ṩ��X��Y�ĵ�һ�����ܵIJ�ֵ��Y��Z�ĵ�һ�����ܵIJ�ֵ�����֪��X��Y��Z��������HԪ�أ���ͬ����Ԫ�����ŵ��Ӳ��������ӣ���һ��������С����X��Y��Z�ֱ�ΪLi��Na��K�����ǽ������ʣ������Խ����������Kԭ�Ӻ˵����Ϊ19��,��������Ų�ʽΪ1s22s22p63s23p64s1���������������������Li��Na��K��1s22s22p63s23p64s1 ����������
��2��BeF2����������ԭ��ΪBe����۵�����Ϊ2��F�ṩ2�����ӣ�����Beԭ�ӵļ۲���Ӷ���Ϊ��2+2��/2=2��Beԭ�ӵ��ӻ�����Ϊsp�ӻ���Ϊֱ���η��ӣ�H2O���ӵ�����ԭ��ΪO����۵�����Ϊ6��H�ṩ2�����ӣ�����Oԭ�ӵļ۲���Ӷ���Ϊ(6+2)/2=4��Oԭ���ӻ�����Ϊsp3��ΪV�η��ӣ��ʴ�Ϊ��sp��sp3��ֱ���Σ�V����
(3)��ԭ�Ӽ۵�����Ϊ3��Cl�ṩ3�����ӣ���ԭ�ӵļ۲���Ӷ���Ϊ(3+3)/2=3����۲���Ӷ���û�й¶Ե��ӣ���BCl3Ϊƽ���������νṹ��������B-Cl���ļ���Ϊ120�㣻����������������ǣ�120�㡣
(4)�ɵ⾧����֪��I2�ھ�����8�������6�����ϣ���һ�������к���4��I2���ӣ�KI������NaCl�����ṹ���ƣ�ÿ��K+����6��I-���������������������4��6��
(5)���ݾ�̯�����㣬K��8��1/8+6��1/2��4��I��12��1/4+1=4�����侧����ԭ����ռ�����V1=(4/3��r3K��4+4/3��r3I��4)��10-30�����������V2=m/��=[4��(MK+M1)]/NA������KI������ԭ�ӵ����ռ��������İٷ���ΪV1/V2��100%= ![]() ��100%������������������ǣ�
��100%������������������ǣ�![]() ��100%��
��100%��

����Ŀ����FeCl3��Al2(SO4)3�Ļ����Һ����μ���Ba(OH)2(aq)���γɳ������������ͼ��ʾ�����������ɵ�pH�����±�(��֪��ƫ���ᱵ������ˮ)�������ƶ���ȷ����

�������� | ��ҺpH | |
��ʼ���� | ������ȫ | |
Fe(OH)3 | 2.3 | 3.4 |
Al(OH)3 | 3.3 | 5.2 |
A. OA�β����ij���ΪBaSO4��Fe(OH)3
B. ��ͼ����ԭ��Һ��c(Cl��)=c(SO42��)
C. AB�ο��ܷ����ķ�Ӧ�ǣ�2SO42��+ 2Ba2++ Al3++3OH��=2BaSO4��+Al(OH)3��
D. C����Һ�ʼ�������ΪAlO2��ˮ�⣬���ӷ���ʽΪ��AlO2��+2H2O=Al(OH)3+OH��
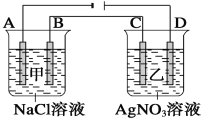
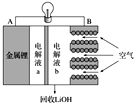
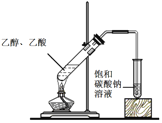
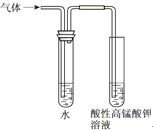
����Ŀ������ʵ�鷽���ܴﵽʵ��Ŀ�ĵ����� ��
��� | A | B | C | D |
ʵ�鷽�� |
|
|
|
|
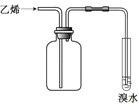
ʵ��Ŀ�� | ʵ�����Ʊ��������� | ���������ˮ | ��֤�����������������Ҵ���Һ�з�����ȥ��Ӧ��������ϩ | �ռ���ϩ����֤������ˮ�����ӳɷ�Ӧ |
A. A B. B C. C D. D