题目内容
【题目】一种正投入生产的大型蓄电系统如图所示。放电前,被交换膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述不正确的是
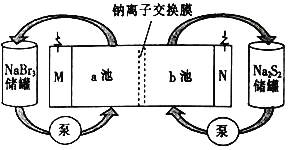
A. 放电时,负极的电极反应式为2S22――2e-===S42-
B. 充电时,阳极的电极反应式为3Br--2e-===Br3-
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 充电时,M接电源负极,N接电源正极
【答案】D
【解析】
根据放电后Na2S2转化为Na2S4,S元素化合价升高,知Na2S2被氧化,说明N为负极;NaBr3转化为NaBr,Br元素化合价降低,知NaBr3被还原,说明M为正极,以此解答。
A. 根据放电后Na2S2转化为Na2S4,S元素化合价升高,知Na2S2被氧化,故负极的电极反应式为2S22――2e-===S42-,故A正确;
B. 充电时阳极发生氧化反应,NaBr转化为NaBr3,故阳极的电极反应式为3Br--2e-===Br3-,故B正确;
C. 放电时,阳离子向正极移动,故Na+经过离子交换膜,由b池移向a池,故C正确;
D. 充电时,原电池的负极接电源的负极,原电池的正极接电源的正极,故M接电源正极,N接电源负极,故D错误。
故选D。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】温度为T时,在两个起始容积都为1 L的恒温密闭容器发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH<0。实验测得:v正=2v(H2)消耗=2v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2(HI),k正、k逆为速率常数,受温度影响。下列说法正确的是
2HI(g) ΔH<0。实验测得:v正=2v(H2)消耗=2v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2(HI),k正、k逆为速率常数,受温度影响。下列说法正确的是
容器 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度 | ||
c(H2) | c(I2) | c(HI) | ||
Ⅰ(恒容) | 0.1 | 0.1 | 0 | c(I2)=0.07 mol·L-1 |
Ⅱ(恒压) | 0 | 0 | 0.6 | |
A. 反应过程中,容器Ⅰ与容器Ⅱ中的物质的量比为1∶3
B. 两容器达平衡时:c(HI,容器Ⅱ)>3c(HI,容器Ⅰ)
C. 温度一定,容器Ⅱ中反应达到平衡时(平衡常数为K),有K=k正/k逆成立
D. 达平衡时,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时v正>v逆