题目内容
【题目】某实验小组同学对电化学原理进行了一系列探究活动。
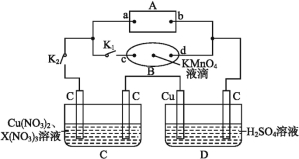
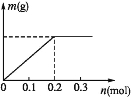
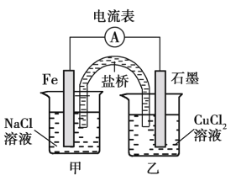
(1)如图为某实验小组依据氧化还原反应_______________(用离子方程式表示)设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差 12 g,导线中通过__________mol 电子。
(2)其他条件不变,若将 CuCl2溶液换为 NH4Cl 溶液,石墨电极发生的电极反应为___________,这是由于 NH4Cl 溶液显_______________(填“酸性”、“碱性” 或“中性”)。用吸管吸出铁片附近的溶液少许置于试管中,向其中滴加少量新制饱和氯水,然后滴加几滴 KSCN 溶液,溶液变红,继续滴加过量新制饱和氯水,溶液颜色褪去,同学们对此做了多种假设,某同学的假设:“溶液中的+3 价铁被氧化为更高价态。” 如果+3 价铁被氧化为 FeO42-,写出发生反应的离子方程式___________________。
(3)其他条件不变,若将盐桥换成弯铜导线与石墨连成的形装置如图所示,一段时间后,在甲装置铜丝附近滴加酚酞溶液,现象是____________,电极反应为__________;乙装置中石墨(Ⅰ)为__________(填“正”、 “ 负” 、 “ 阴”或“阳”)极。
【答案】(1)Fe+Cu2+=Fe2++Cu(2分)0.2(2分);
(2)2H++2e-=H2↑(2分)酸性(2分)
2Fe3++3Cl2+8H2O=2FeO42+6Cl-+16H+(2分);
(3)溶液变红(2分)O2+2H2O+4e-=4OH-
【解析】
试题分析::(1)图1为原电池反应,Fe为负极,发生:Fe-2e-=Fe2+,石墨为正极,发生Cu2++2e-=Cu,总反应式为Fe+Cu2+=Fe2++Cu;一段时间后,两电极质量相差12g,则
Fe+Cu2+=Fe2++Cu 两极质量差△m 转移电子
56g 64g 56g+64g=120g 2mol
12g n
则:n=0.2mol。
(2)若将CuCl2溶液换为NH4Cl溶液,溶液呈酸性,发生:NH4++H2O![]() NH3H2O+H+,负极发生2H++2e-═H2↑,负极发生反应:Fe-2e-=Fe2+,加入氯水发生反应:2Fe2++Cl2═2Fe3++2Cl-;如果+3价铁被氧化为FeO42-,发生反应为:2Fe3++3Cl2+8H2O=2FeO42+6Cl-+16H+;
NH3H2O+H+,负极发生2H++2e-═H2↑,负极发生反应:Fe-2e-=Fe2+,加入氯水发生反应:2Fe2++Cl2═2Fe3++2Cl-;如果+3价铁被氧化为FeO42-,发生反应为:2Fe3++3Cl2+8H2O=2FeO42+6Cl-+16H+;
(3)若将盐桥换成弯铜导线与石墨相连成n型,甲装置为铁的吸氧腐蚀,铁为负极,铜为正极,正极发生 O2+2H2O+4e- =4OH-,呈碱性,滴加酚酞,溶液变红,则乙装置铜为阳极,石墨为阴极,乙为电解池装置,阳极发生2Cl--2e-═Cl2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )
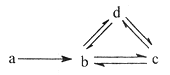
a | b | c | d | |
① | Si | SiO2 | H2SiO3 | Na2SiO3 |
② | N2 | NO | NO2 | HNO3 |
③ | Cu | CuO | Cu(OH)2 | CuSO4 |
④ | Na | NaOH | Na2CO3 | NaHCO3 |
A.①② B.②③ C.③④ D.②④
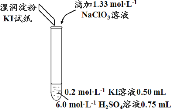
【题目】某实验小组同学模拟工业制碘的方法,探究ClO![]() 和I
和I![]() 的反应规律。实验操作及现象如下:
的反应规律。实验操作及现象如下:
实验及试剂 | 编号 | 无色NaClO3 溶液用量 | 试管中 溶液颜色 | 淀粉KI 试纸颜色 |
| 1 | 0.05 mL | 浅黄色 | 无色 |
2 | 0.20 mL | 深黄色 | 无色 | |
3 | 0.25 mL | 浅黄色 | 蓝色 | |
4 | 0.30 mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如下实验:
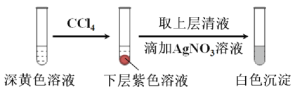
经检验,上述白色沉淀是AgCl。写出加入0.20 mL NaClO3后,溶液中ClO3-和I-发生反应的离子方程式: 。
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-。
作出假设: NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2。
进行实验:
①取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有IO3-。
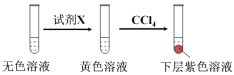
其中试剂X可以是 (填字母序号)。
a.碘水 b.MnO4溶液 c.NaHSO3溶液
② 有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30 mL 1.33 mol·L1 NaClO3溶液后,发现湿润的淀粉试纸没有明显变化。进行以上对比实验的目的是 ,进一步佐证实验4中生成了Cl2。
获得结论:NaClO3溶液用量增加导致溶液褪色的原因是 (用离子方程式表示)。
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如下实验结果:
编号 | 6.0 mol·L1 H2SO4溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
5 | 0.25 mL | 浅黄色 | 无色 |
6 | 0.85 mL | 无色 | 蓝色 |
①对比实验4和5,可以获得的结论是 。
②用离子方程式解释实验6的现象: 。